
(#101)
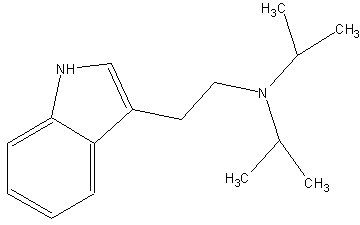
N,N-Diisoproypltryptamin, DIT. (#62/181) TRYPTAMINE, N,N-DIISOPROPYL; INDOLE, 3-[2-(DIISOPROPYLAMINO)ETHYL]; N,N-DIISOPROPYLTRYPTAMINE; 3-[2-(DIISOPROPYLAMINO)ETHYL]INDOLE; (#101/403)
30 mg oral (Usenet) 25 - 100 mg, oral (#101/404)
6 - 8 h. (#101)
Diese Verbindung ist von der chemischen Struktur her ein Tryptamin und damit nahe verwandt mit anderen hoechst psychoaktiv wirksamen Verbindungen, wie Psilocybin, Psilocin oder auch DMT. (eigen)
Die Verbindung ist halluzinogen, wie Untersuchungen von Szara 1957 und von Szara und Hearst im Jahr 1962 ergaben. Alexander Shulgin untersuchte das Halluzinogen 1976 und stellte eine geringe orale Wirksamkeit fest. (#62/181)
Die Droge aendert hauptsaechlich das Hoersystem im Gehirn des Menschen, das Verzerrungen von Musik und Sprache wahrnimmt. (#101/405f.)
Alexander Shulgin fuehrt in Thikal folgende Subjektiven Wirkungsbeschreibungen an:
(mit 18 mg, oral) "Wilde Wirkungen werden in einer Stunde bemerkt. Bemerkenswerte Aenderungen in der Musikwahrnehmung. Die Stimme meiner Frau ist mit Bass, wie wenn sie verkuehlt waere -- so wie wenn meine Ohren mit leichten Druck verstopft waeren, aber sie sind es nicht. Radiostimmen sind alle niedrig, Musik ist ausserhalb des Notenschluessels. Pianotoene sind wie ein Barraumdisaster. Der Telephonklingelton klingt, wie wenn er teilweise unter Wasser waere. In einigen Stunden ist die Musik wieder normal.
(mit 50 mg, oral) "Alles war ein Konzert, und ich kann es nur mit einem '!' beschreiben."
(mit 100 mg, oral) "Nichts bis in 35 Minuten, als es einen ausgepraegten Wechsel im Hoeren gab. Es gab einen Abfall in hohen Frequenzen mit einer unueblichen Tonverschiebung von allen Frequenzen zu einer niederen. Stimmen klangen sehr aehnlich zu einem einseitig angebundenen Radiosignal, welches verstimmt war hin zu den niederen Frequenzen. Alle familiaeren Sounds wurden fremd, das Kauen von Essen eingeschlossen. Keine Wirkungen wurden bemerkt zur Klarheit der Sprache und beides - Begriffsvermoegen und Interpretation waren normal. Musik war komplett disharmonisch verstimmt, obwohl einzelne Toene normal klangen. Es gab keine Wechsel in der Vision, im Geschmack, Geruch, Appetit, Vitalsignalen oder der Motorkoordination. Die Wirkungen begannen nach 4 Stunden langsam nachzulassen und waren nach acht Stunden komplett verschwunden. Milder Durchfall tauchte von der fuenften zur 10.ten Stunde auf, war aber kein nennenswertes Problem. (#101/404f.)
Es ist keine Ausbildung einer koerperlichen oder psychischen Abhaengigkeit bekannt. (eigen)
Aus dem Werk TIHKAL von Alexander und Ann Shulgin wurden folgende zwei Synthesen entnommen:
(von Indol aus) Zu einer gut geruehrten Loesung von 10 g Indol in 100 mL MTBE, abgekuehlt auf 0 Grad Celsius mit einem Eisbad, wurden 8.6 g Oxalylchlorid hinzugefuegt. Die Reaktionsmischung wurde 0.5 h lang geruehrt, und die Feststoffe wurden durch Filtration entfernt und wurden zweimal mit 50 mL MTBE gewaschen. Dieses Saeurechlorid wurde zu 20 mL wasserfreiem Diisopropylamin hinzugefuegt. Es wurde dann ein Ueberschuss an an 2N HCl hinzugefuegt, die Mischung gekuehlt, und die resultierenden Feststoffe wurden durch Filtration entfernt. Diese wurden aus MeOH umkristallisiert, um nach Lufttrocknen 11.4 g (49%) Indol-3-yl-N,N-diisopropylglyoxylamid mit einem Schmelzpunkt von 200-202 Grad Celsius zu ergeben.
Eine Loesung von 11 g Indol-3-yl-N,N-diisopropylglyoxylamid in 350 mL wasserfreiem Dioxan wurde hinzugefuegt zu 19 g LAH in 350 mL Dioxan, welches gut geruehrt wurde und auf Rueckflusskochtemperatur unter einer Inertathmosphaere gehalten wurde. Nachdem die Addition komplett war, wurde das Kochen am Rueckfluss 16 h lang aufrechterhalten. Die Reaktionsmischung wurde abgekuehlt, und das ueberschuessige Hydrid wurde zerstoert durch die vorsichtige Zugabe von nassem Dioxan. Die gebildeten Feststoffe wurden durch Filtration entfernt, gewaschen mit heissem Dioxan, die Filtrate und Waschungen wurden kombiniert, getrocknet ueber wasserfreiem MgSO4, und das Loesungsmittel wurde unter Vakuum entfernt. Der Rest wurde in wasserfreiem Et2O geloest und gesaettigt mit wasserfreiem Wasserstoffchlorid. Es bildeten sich Kristalle aus Benzol/Methanol, um 4.5 g (40%) N,N-Diisopropyltryptaminhydrochlorid (DIPT) mit einem Schmelzpunkt 198-199 Grad Celsius zu ergeben. (#101/403f.)
(von Tryptamin aus) Eine Loesung von 1.60 g Tryptaminbase in 10 g geschmolzenen Sulfolan wurde mit 8.5 g Isopropyliodid und 6.5 g Diisopropylethylamin behandelt, und auf Dampfbadtemperatur 12 h lang mit gelegentlichen Schuetteln gehalten, um die 2 Phasen zu mischen. Diese Mischung wurden dann zu 100 mL H2O hinzugefuegt, und mit drei 30 mL Portionen Hexan extrahiert. Diese Fraktionen wurden kombiniert und nach dem Entfernen des Loesungsmittels unter Vakuum wurde der Rest in einem Kugelrohrapparat destilliert, um ein blass weisses Oel zu ergeben, dass bei 170-185 Grad Celsius mit einem Druck von 0.05 mm/Hg kochte und 1.37 g (56%) wog, dass spontan zu einem Feststoff kristallisierte mit einem Schmelzpunkt von 69-71 Grad Celsius. Umkristalliesieren einer Probe aus Hexan erzeugte ein weisses Produkt mit einem Schmelzpunkt von 72-74 Grad Celsius. Eine Loesung von 0.50 g der freien Base in 2.5 mL Isopropanol wurde mit 0.5 mL konzentrierter HCl behandelt und langsam verduennt mit Et2O unter starkem Ruehren. Es wurden so, nach Filtrieren, Waschen und Lufttrocknen, das Hydrochloridsalz mit einem Schmelzpunkt von 192-193 Grad Celsius erhalten. (#101/403f.)
1957: Szara untersuchte DIPT und stellte eine halluzinogene Wirksamkeit fest. (#62/181)
1962: Szra und Hearst testeten das Halluzinogen DIPT. (#62/181)
1976: Alexander Shulgin untersucht DIPT und stellte eine geringe, orale Wirksamkeit fest. (#62/181)
Abbildung 1: In: TRACHSEL Daniel, RICHARD Nicolas: "Psychedelische Chemie.", S. 356, Nachtschatten Verlag, Solothurn, 2000.