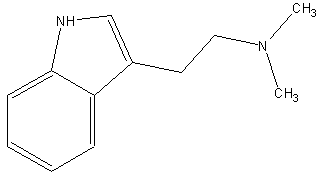

(#8, #57, #62/433)
(2-(3-Indolyl) -N,N- dimethylethylamin, (#12) N,N- Dimethyltryptamin, (#12, #36, #62/433) 3-[2-(Dimethylamino) ethyl] indol, (#62/433) Dimethyltryptamin, (#12, #46, #62/433) Nigerin. (#11, #57, #62/433) N,N-Dimethyltryptamine (engl.), N,N-Dimethyl-1H-indole-3-ethanamine (engl.), 3-[2-(dimethylamino)ethyl]indole /engl.), DMT. (MerckIndex)
N,N-Dimethyltryptamine, 1H-Indole-3-ethanamine, N,N-dimethyl-; Indole, 3-[2-(dimethylamino)ethyl]-; 2-(3-Indolyl)ethyldimethylamine; 3-(2-Dimethylaminoethyl)indole; Dimethyltryptamine; DMT; 2-(1H-Indol-3-yl)-N,N-dimethylethanamine; Dimethyltryptamine (dmt); N,N-dimethyl-1H-indole-3-ethylamine. (NIST)
DMT wird ueblicherweise benutzt und gelagert als Fumarat, weil andere DMT Saeuresalze sind allgmemein sehr hygroscopisch sind und nicht gut kristallisieren. Die Freebase Form, obwohl weniger stabil als DMT fumarat, wird bevorzugt bei Konsumenten zum Rauchen, weil sie einen niederen Siedepunkt hat. Im Gegensatz zur DMT's Base, sind seine Salze wasser-loeslich. DMT in Loesung zersetzt sich relativ schnell und sollte geschuetzt von Luft, Licht und Hitze in einem Gefrierschrank gelagert werden. (Wikipedia)b
Freebase DMT:
Aussehen: Weisse/Transparente (DMT-Nexus, tryptamind) (unreine Formen koennen gelb sein) (tryptamind) Kristalle; (MerckIndex 13. Aufl., tryptamind)
CAS Registry Number: 61-50-7; (MerckIndex 13. Aufl., DMT-Nexus)
Schmelzpunkt: 44,6-44,8 Grad Celsius; (MerckIndex 13. Aufl.)
Schmelzpunkt: 44.6-46.8 Grad Celsius; (tryptamind)
Schmelzpunkt: 46 Grad Celsius; Platten aus Ethanol und light petroleum, Benzin berichtet Fleming und Woolias; (MerckIndex 13. Aufl.)
Schmelzpunkt: 44-68 Grad Celsius (Wiedersprechende Berichte in der Literatur, in TIHKAL berichtet); (DMT-Nexus)
Siedepunkt: 60-80 Grad Celsius; (MerckIndex 13. Aufl.)
Summenformel: C12H16N2; (DMT-Nexus)
Molgewicht: 188.26884 g/mol; (DMT-Nexus)
Zusammensetzung: C 76.55%, H 8.57%, N 14.88%; (MerckIndex 13. Aufl.)
XLogP: 2.0; (DMT-Nexus)
XLogP3: 2.5; (PubChem, DMT-Nexus)
pKa: 8.68; (Ethanol-Wasser); (MerckIndex 13. Aufl., DMT-Nexus)
Stabilitaet/Zerfall: Oxidation zu DMT N-Oxid (gelbes Oel, kristallisiert nicht!) in extensiver Gegenwart von Sauerstoff (besonders beim Verdampfen von DMT-beinhaltenden Loesungsmitteln mit Hitze und/oder Foehn oder allgemein bei laengerem Kontakt mit frischer Luft). DMT-N-oxid kann zurueckgewandelt werden zur Mutterverbindung durch Reduktion, wie beschrieben wurde; (DMT-Nexus)
Loeslichkeit:
Sehr loeslich in Xylen, Toluol, Limonen, Aceton, IPA, Methanol, Ethanol, DCM, Chloroform, Aether, MEK, Butanol; (DMT-Nexus)
Frei loeslich in verd. Essigsaeure (MerckIndex, Wikipedia) und verd. Mineralsaeuren; (MerckIndex 13. Aufl.)
Loeslich in Naphtha/Benzin, Hexan, Heptan aber beinahe unloeslich in diesen Loesungsmitteln bei Gefrierfachtemperaturen; (DMT-Nexus)
Beinahe unloeslich in Wasser; (DMT-Nexus)
Unloeslich in Wasser. (tryptamind)
DMT Fumarat:
Molgewicht: 492.608 g/mol;
Schmelzpunkt: 152-152,5 Grad Celsius; (#62/433)
Loeslichkeit:
Sehr loeslich in Wasser;
Loeslich in siedendem IPA, praktisch unloeslich bei Raumtemperatur IPA (~1mg/ml);
Loeslich in Methanol (~10mg/ml);
Sehr leicht loeslich in Ethanol (~5mg/ml);
Unloeslich in gefrier-kaltem IPA;
Unloeslich in gefrier-kaltem Aceton;
Unloeslich in FASI (Fumarsaeure gesaettigtes IPA);
Unloeslich in FASA (Fumarsaeure gesaettigtes Aceton). (DMT-Nexus)
DMT Methiodid:
Schmelzpunkt: 216-217 Grad Celsius; (MerckIndex, #62/433)
DMT Pikrat:
Schmelzpunkt: 169.5-170 Grad Celsius; (#62/433)
DMT Hydrochlorid:
Hygroskopisch; (tryptamind)
Schlecht kristallisierbar! (Shulgin, TIHKAL)
DMT Acetat:
Loeslichkeit: gut in chlorierten Kohlenstoffen!
Beim Extrahieren: Essigsaeure und chlorierte Loesungsmittel, wie z.Bsp. DCM (Dichlormethan), vertragen sich nicht! (Internet)
Acacia angustissima, A. berlandieri, A. colei, A. confusa, A. jurema, A. laeta, A. longifolia, A. maidenii, A. melanoxylon, A. mellifera, A. nilotica, A. nubica, A. obtusifolia, A. oerfota, A. plebophylla, A. podalyriaefolia, A. polyacantha, Acacia retinodes, Acacia rigidula, A. senegal, A. sieberiana, A. simplicifolia, Acacia suma, A. tortilis;
Albizia inundata;
Amanita citrina;
Anandenanthera colubrina, A. excelsa, A. peregrina;
Arundo donax;
Banisteriopsis muricata, B. rusbyana;
Delosperma acuminatum, D. cooperi, D. ecklonis, D. esterhuyseniae, D. harazianum, D. hirtum, D. lydenbergense, D. pageanum D. pergamentaceum, D. tradescantioides;
Desmanthus illinoensis, D. leptolobus;
Desmodium caudatum, D. gangeticum, D. gyrans, D. pulchellum, D. tiliaefolium, D. triflorum;
Justicia pectoralis var. stenophylla;
Lespedeza bicolor;
Mimosa hostilis (C. Martius) Bentham, M. nigra Huber, M. ophthalmocentra, M. scabrella, M. tenuiflora, M. verrucosa Bentham;
Mucuna pruriens;
Osteophloem platyspermum;
Pandanus (unsicher);
Petalostylis casseoides, P. labicheoides;
Phalaris arundinaceae, P. tuberosa;
Phragmites australis;
Testulea gabonensis;
Trichocereus terschekii;
Vepris ampody;
Virola calophylla,
V. calophylloidea, V. carinata, V. divergens, V. melinonii, V. pavonis, V. peruviana, V. rufula, V. sebifera, V. theiodora, V. venosa;
Zanthoxylum arborescens, Z. procerum.
DMT ist ein natuerlich vorkommendes Halluzinogen, dass aber auch synthetisch hergestellt werden kann und manchmal auch wird. Es ist von der chemischen Struktur her ein Tryptamin und kommt am ehesten als DMT-fumarat in den Handel. Es ist von der Struktur her nahe verwandt mit dem bekannten Pilzwirkstoff Psilocybin, aber auch den Nebenalkaloiden Psilocin und Baeocystin der sogenannten "magic mushrooms", welche ebenfalls von ihrer chemischen Struktur Halluzinogene Tryptamine sind. Man kann DMT als Stammsubstanz dieser Gruppe von Halluzinogenen auffassen, denn von der chemischen Struktur ist es das einfachste, halluzinogen wirksame Tryptamin, dass es gibt. Das Tryptamin ist uebrigens selber nicht halluzinogen. Von der Strukturformel unterscheidet es sich vor allem durch die Substitution an der 4. Position, von anderen Halluzinogenen, aber es gibt auch Variationen, die sich durch Veraenderungen an der Amingruppe auszeichnen. Je nachdem welche Molekuelgruppe an der 4. Stelle gebunden sind, ergeben sich so bekannte Halluzinogene, wie das erwaehnte Psilocybin, aber auch Psilocin, dass auch ein bekannter Wirkstoff der halluzinogenen Pilze der Gattung Psilocybe und auch anderer ist. Werden andererseits die beiden Methylgruppen, die am Stickstoffatom am Ende der Seitenkette gebunden ist, durch zwei Ethylgruppen ausgetauscht, ergibt sich das bekannte Halluzinogen DET (Diethyltryptamin). Verlaengerungen in diesen Seitenketten fuehren zu einer Verlaengerung der Wirkung, welche beim DPT (Dipropyltryptamin) gut erkennbar ist. Grundsaetzlich sind die einzelnen halluzinogenen Tryptamine in ihrer Wirkung aehnlich, unterscheiden sich aber in ihrer Wirkdauer und der Intensitaet der Erfahrung voneinander. Die Aufklaerung grundsaetzlicher Strukturwirkungszusammenhaenge von tryptaminergen Halluzinogenen, einer kleinen Molekuelgruppe der Pflanzenalkaloide, ist durch die Arbeiten von A. Shulgin v.a. in seinem Buch TIHKAL geschehen. (eigen)
DMT ist auch nahe verwandt mit Serotonin, einem Neurotransmitter des menschlichen Gehirns, welcher dort eine bedeutende Rolle spielt. Serotonin ist nichts anderes als 5-Hydroxytryptamin und damit sehr nahe chemisch mit DMT und anderen halluzinogenen Tryptaminen verwandt. Dies gab und gibt zu einer Reihe von Spekulationen und Theorien Vorschub, welche alle noch einer ausreichenden Untersuchung harren. Es wurde lange vermutet, dass eine halluzinogene Wirkung durch Beeinflussung dieses Neurotransmitter-Schaltkreises im Gehirn verursacht wird. Doch die neuere psychopharmakologische und klinische Forschung hat Medikamente entwickelt, die genau diesen Schaltkreis hemmen, und man nennt solche Verbindungen dann Serotoninhemmer, oder auch Serotonin-antagonisten. Eigentlich muessten halluzinogene Symptome aufhoeren, oder sich wesentlich abschwaechen, wenn man Serotoninantagonisten an Menschen verabreicht, doch dies ist nur teilweise der Fall, ebensowenig verursachen Substanzen, die sich anstelle von Serotonin an den Serotonin-Neurorezeptor binden "halluzinogene Symptome". Der Serotonin-Schaltkreis teilt sich in viele verschiedene Unterrezeptoren auf. Die klinische Forschung zeigt auf, dass eine Beeinflussung des Serotoninstoffwechsels im Zusammenhang mit der Entwicklung von Depressionen steht und eine Reihe von klinisch verwendeten Antidepressiva, verdankt ihre Wirkung der Beeinflussung des Serotoninsystems, aber auch ein Zusammenhang mit bestimmten visuellen Phaenomenen der Halluzinogenwirkung besteht und wird ueber bestimmte Serotonin-unterrezeptoren vermittelt. Diese wurden vor allem im vorderen Cortex des Gehirns lokalisiert. Diese Informationen stammen aus dem Buch "Therapie mit psychoaktiven Substanzen" von H. Jungaberle et al. (eigen)
Synthetisches DMT (Dimethoxytryptamin) ist uebrigens auf dem Schwarzmarkt in Europa und Amerika, und ganz speziell in Oesterreich, so gut wie nicht zu finden. Als Quelle der Substanz dienen am ehesten noch Pflanzen, aus denen durch Extraktion oder Bereitung in Teeform das Halluzinogen gewonnen wird. DMT ist eine gefragte, aber seltene Rauschdroge. (eigen)
Die bekannteste Bereitung, welche DMT enthaelt ist ayahuaska, ein in Suedamerika gebrauechliches Gebraeu, welches dort eine wesentliche Rolle in der Kultur der am Amazonasgebiet lebenden Indianer darstellt. Diese Droge wird grundsaetzlich aus einer DMT-haeltigen Pflanze und Verbindungen, die die Monoaminoxidase (MAO) hemmen, hergestellt. (#32, #57, #62) Im Amazonasgebiet dienen zur MAO-Hemmung vor allem beta-Karbolinalkaloide, die auch aus Pflanzen gewonnen werden. Zur Bereitung von ayahuaska werden, unterer anderem, Banisteriopsis-Arten verwendet. So enthaelt B. rusbyana DMT und B. caapi die notwenigen beta-Karbolinalkaloide, um die Droge auch oral wirksam zu machen, denn DMT alleine kann nicht durch den Magen aufgenommen werden. Doch Banisteriopsis-Arten sind nicht die einzige Quelle von DMT am Amazonas: Auch die Pflanze Psychotria viridis wird zur Bereitung des Rauschgetraenkts verwendet, und enthaelt ebenso DMT. (#57, #62)
Von dieser Zubereitung, deren Gebrauch vor allem auf Suedamerika und auch Australien beschraenkt ist, haben sich laut Jonathan Ott eine Reihe von anderen moeglichen und neuen Bereitungsformen von "ayahuaska", die das selbe Wirkprinzip enthalten, abgeleitet. Es wird zum Beispiel auch eine Bereitung unter dem Namen acaciahuaska verwendet, die australischen Ursprungs ist. Hierzu werden dort einheimische Pflanzen der Gattung Acacia und die Samen von Peganum harmala (der Steppenraute) verwendet, denn manche Acacia-Arten enthalten auch DMT und Peganum harmala ist jene Pflanze, welche die groesste Menge an beta-Karbolinalkaloiden enthaelt. (#57, #62)
Jonathan Ott fuehrte auch die Bezeichnung pharmahuaska ein - fuer synthetisches oder extrahiertes DMT mit einem pharmazeutisch verwendeten MAO-Hemmer. Es wurden dazu Kombinationen mit Medikamenten vom Typ der Antidepressiva getestet. Die MAO-hemmenden Antidepressiva (es gibt Antidepressiva, deren Wirkung nicht auf einer Hemmung der Monoaminoxidase beruht!) erwiesen sich als wirksam. Der einzige Unterschied ist, dass sie im Gegensatz zu den beta-Karbolinalkaloiden die Monoaminoxidase ueber eine laengere Zeit irreversibel hemmen. (#57, #62)
Aus Berichten aus dem Internet wurde entnommen, dass nun auch Anadenanthera-Arten die Quelle einer ayahuasa-Bereitung verwendet werden, dass sie auch DMT-haeltig sind - aber der Hauptinhaltsstoff ist eigentlich Bufotenin, wie wir aus neueren Studien sicherlich wissen. Also muss dieses Alkaloid auch durch MAO-Hemmer verstaerkt werden, und oral konsumierbar werden oder sein. Als MAO-Hemmer wird vor allem Peganum harmala (Harmal, Steppenraute) verwendet in Europa verwendet. (eigen)
Ayahuaca ist jedoch nicht die einzige natuerliche Bereitung, die Dimethoxytryptamin enthaelt und gebrauechlich ist, denn der halluzinogene Pflanzeninhaltsstoff DMT ist eine weitverbreitete Substanz. In Form des Schnupfpulvers epena wird die Droge weitverbreitet und kulturell integriert am Amazonas gebraucht, insofern der Urwald und die darin lebenden Menschen noch existieren. Fuer die Bereitung von epena werden uebrigens verschiedene Virola-Arten verwendet, die sich durch einen Gehalt an DMT, aber auch an dem sehr aehnlich wirkenden 5-Methoxy-DMT, auszeichnen. (#12, #57, #62, &1) Doch diese Virola-Arten, bestimmte Arten davon die staerkste, bekannte Quelle des Halluzinogens sind, doch diese sind kaum in der westlichen Welt bekannt und gehoeren noch zu den wenig erforschten Quellen halluzinogener Drogen, die immer noch in Suedamerika den dortig lebenden Menschen vorbehalten sind. (eigen)
Weiters wurde die Substanz auch aus den Samen der Gattung Anadenanthera gewonnen und ist seit kurzem auch wieder als hoechst seltene Droge kaeuflich zu erwerben. Diese Schnupfpulver tragen den Namen yopo oder cohoba. Cohoba war uebrigens der alte Name auf den Westindischen Inseln, yopo ist die Bezeichnung des Halluzinogens im kontinentalen Suedamerika, wo der Gebrauch heute noch anzutreffen ist. Der Gebrauch von Cohoba scheint ausgestorben zu sein. Cohoba wird aus A. colubrina und einer Varietaet gewonnen, beinhaltet aber hauptsaechlich Bufotenin und nur Spuren von DMT! Davon koennen wir ableiten, dass Bufotenin aehnlich wie DMT wirkt. Es ist auch stark halluzinogen wirksam, wie wir bewiesen haben. Cohoba ist eigentlich staerker als yopo. Yopo wird aus Anadenanthera peregrina-Arten und manchen Varietaeten gewonnen. (#12, #57, #62, &1)
Erst durch den Einsatz von Ethnobotanikern und Reisenden konnten Samen und Pflanzen in die westliche Kultur gebracht werden, wo diese seit kurzem kaeuflich erwerbar sind. (&1) Es sind dies vor allem die bereits obenangefuehrte Pflanzen, beispielsweise Samen der Gattung Anadenanthera, diverse australische Acacia-Arten, Banisteriopsis-Arten, Psychotria viridis, welche den Grundstock der Verbreitung von DMT in der amerikanischen und europaeischen Welt bilden. (#57/62)
Aber auch die bei uns heimische Pflanze Phalaris arundinaceae, eine Grasart, welche ebenso DMT enthaelt, dient seit kurzen als Quelle fuer diverse Drogenbereitungen. (#57, #62) Diese Pflanze wird aber bei uns in Oesterreich noch nicht als Halluzinogen verwendet und ist noch kaum bekannt, ebenso wenig wird sie derzeit in Jugoslawien oder Italien breiter genutzt, wo sie haeufig vorkommt. Das Kerngebiet der Ausbreitung der Pflanze ist in der italienischen Poebene gelegen. Dass Phalaris-Arten als Halluzinogene benutzt werden koennen ist eine relativ neue und noch kaum publizierte Theorie - im Gegensatz zu den obengenannten Rauschbereitungen, die schon seit Jahrhunderten in Gebrauch sind. In den letzten Jahren sind einige Arbeiten ueber diese Pflanze erschienen, so wird ihr Gehalt an DMT in Studien genauestens untersucht und dargestellt. Ebenso werden die anderen, weniger bekannten Phalaris-Arten untersucht. Eine der Untersucher waren FESTI Francesco & SAMORINI Giorgio: "Ayahuasca-Iike" effects obtained with Italian plants", Communication presented at the 11th International Congress for the Study of the modified States of Consciousness, 3-7 October 1994, Lleida (Espania); diese sehr saubere und gelungene Arbeit ist auch in unserer OnLineBibliothek als Primaerquelle enthalten. (eigen)
Aufgrund seiner geringen Wirkdauer ist die Verbindung DMT sicherlich nicht geeignet fuer den Konsum bei Raveveranstaltungen, noch ist es geeignet fuer tiefgreifende psychoanalytische Sitzungen, da seine Wirkungen sehr schnell, meist nach einer Viertelstunde, verblassen. DMT ist als Halluzinogen nur fuer eine sehr kurze, intensive visuelle Erfahrung geeignet. DMT wird vermutlich von den meisten Konsumenten immer wieder aufeinanderfolgend in Purpfeifenform genossen werden. Dies nennt man auf English "redosing". (eigen)
DMT ist uebrigens auch schon seit Existenz der "single convention" (Einheitsuebereinkommen der UN) verboten und leider damit in den meisten Laendern dieser Welt bereits illegalisiert worden, bevor dieses Halluzinogen ueberhaupt ausreichend auf seine Wirkung und Gefaehrlichkeit untersucht werden konnte. DMT ist im Zuge des Verbots halluzinogener Rauschdrogen, v.a. LSD verboten worden, da die damals durchgefuehrten Studien auf eine nahe Verwandtschaft zu diesem Halluzinogen hindeuteten. Das Verbot von DMT passt nicht zur Harmlosigkeit der Substanz, so fehlt dem DMT die umstrukturierenden auf die Psyche einwirkenden Kraefte, die LSD einerseits so hilfreich in der substanzunterstuetzten Psychotherapie, aber auch andererseits sehr gefaehrlich bei Missbrauch erscheinen lassen. LSD muss man lenken, DMT kann man treiben lassen. (eigen)
DMT unterscheide sich von LSD physisch durch eine staerkere koerperliche Veraenderung, v.a. eine gelegentlich massive Blutdrucksteigerung (um bis zu 70mm Hg) und extrapyramidale Bewegungsstoerungen, die denen der Parkinson-Krankheit aehneln (fahrige Gesten, Grimassieren, Zuckungen der Glieder, tonische Kraempfe, langsam-gespreizte Bewegungen.) Diese Bewegungsstoerungen beruhen darauf, dass DMT offensichtlich auch die "basalen Stammganglien" angreift, die im Zwischen- und Mittelhirn liegen und die unwillkuerliche Koerperhaltung sowie die unwillkuerliche Mitbewegungen der Glieder, etwa beim Gehen regeln. Behaupten die Autoren des "Handbuchs der Rauschdrogen", J. vom Scheidt und W. Schmidbauer. (#13) (Diese Wirkungen wurden aber von mir niemals beobachtet. Eigene Untersuchungen mit DMT zeigte diese Eigenschaften, wenn man DMT raucht, nicht. Es entsteht der Verdacht, dass dies Eigenschaften der i.v. Konsumform sind. Eine eindeutig beim cohoba-Schnupfpulver auftretende Uebelkeit, die meist vor Beginn der eigentlichen halluzinogenen Wirkung auch noch Erbrechen ausloest, ist beobachtbar, wird aber von DMT alleine nicht verursacht, noch wird sie vom Hauptinhaltsstoff Bufotenin verursacht, wie Untersuchungen durch Psychonauten ergeben haben! Dies wurde schon von J.OTT angemerkt und fuehrt auf DMT-Nexus zu einer Reihe von Untersuchungen, damit die Stoffe in den Anadenanthera-Arten bestimmt werden, die fuer diese Wirkung verantwortlich sind. (eigen)
Der Rauschzustand ist aehnlich dem, der von LSD ausgeloest wird. Dabei scheinen die Leuchtkraft der Farbvisionen und die Eindringlichkeit der optischen Pseudohalluzinationen besonders stark erlebt zu werden, auch die Wirkung auf Stimmung, Affekt und Gefuehl ist staerker ausgepraegt als bei LSD, wird da behauptet. (#12)
Nach eigenen Untersuchungen und Erfahrungen ist der DMT-trip zwar aehnlich dem LSD, aber grundsaetzlich qualitativ verschieden. DMT fehlt die dem LSD so typische psychisch umstrukturierende, psychodynamischen Wirkungen, die LSD fuer die psychedelische Therapie brauchbar machen, doch die Wirkung von DMT ist fuer eine Psychotherapie zu kurz und zu visuell autark ablaufend, ohne dass man die lange-hin-und-her schwankende LSD-Erfahrung vergleichen koennte. (eigen)
Es gibt eine rasche Entwicklung einer Toleranz, die jedoch auch schnell wieder verschwindet. Aus den Untersuchungen von Rosen et al. aus dem Jahr 1964 geht hervor, dass DMT mit LSD eine Kreuztoleranz aufweist, die jedoch nach den Forschungsarbeiten von Brown aus dem Jahr 1968 sicherlich nach 4 Stunden wieder vergangen ist. (#62/181)
Erfahrungen mit gerauchtem DMT, dass besonders kurz in seiner Wirkung ist, zeigten vor allem Pseudohalluzinationen mit geschlossenen Augen, die beim Oeffnen der Augen sofort verschwanden. Mit geschlossenen Augen sieht man bunte Muster, reale Orte, stark intensivierte Farbwahrnehmungen, Personen, die mit einem sprechen, sogenannte entitities (Entitaeten), deren Beratung sich in dem Ausdruck "die Pflanzengeister sprechen zu dir" sich aeussert, diesen Ausdruck gebrauchen die Eingeborenen Suedamerikas fuer die Wirkungsgeschreibung, und in der Praxis in total kognitiv-klare und verstaendliche Instruktionen, durch diese entitities, die da ganz moralin-sauer beraten. Das da mehr als ein Ich im Kopf spricht, bringt natuerlich mal wieder den Begriff der "Modellpsychose" sicherlich ans Licht, der den fruehen Formulierungsversuchen und Begriffsfassen etwas zu frueh entsprungen ist, und den komplexen Zustand der Erfahrung mit den organisch-verursachten und teilweise auch kognitiv-verwirrten Zustaenden verglich, die echte Schizophrene aufweisen, die sprachliche Formulierungsprobleme und Assoziationskettenrisse sporadisch aufweisen, die der klaren und kognitiv-ungestoerten DMT-Erfahrung nicht entspricht. Selbst bei extrem ueberdosierten, stark visuell gepraegten DMT-Erfahrungen, treten kognitive Stoerungen nicht auf, aber starke Filmszenen mit offenen Augen auf, die ungemein heftig sind. Todeserfahrungen, Ahnenkontakte, die sich zum Beispiel in Gespraechen mit "real" ansprechbaren innerlichen verstorbenen Familienmitgliedern aeussern, zeigen die ungemein psychodynamisch kraftvolle Erfahrung auf, die energetisch ungemein reaktiv ist, und eine individuelle Nutzbarmachung offenbaren, die man sich selbst vermitteln muss in Konfrontation mit der Substanz und ihren Auswirkungen auf sich in der jeweiligen Lebenssituation. Lernen muss man den Lehrstoff in den Schulen und Universitaeten auch alleine, so ist es auch mit der psychedelischen Erfahrung, ihrer spezifischen Individualitaet, und Anleitung kann nur vorbereitend sein, jedoch nicht aeusserlich lenkbar ist, wenn sie mit voller Kraft ablaeuft und eine Selbstreparturfaehigkeit der Natur offenbart, die DMT innewohnt. (eigen)
Das Halluzinogen DMT ist stark wirksam und erzeugt eine so intensive Wirkung, dass es den Konsumenten regelrecht auf den Boden wirft, damit ist es mehr als empfehlenswert sich niederzusetzen, wenn man die Droge appliziert. Dies duerfte aber nur fuer die Schnupfpulverapplikationen gelten, deren Konsumform und Konzentration vor allem von cohoba von uns untersucht wurde und es wird von uns bestaetigt, dass diese wirklich eine umwerfend starke Wirkung haben, aber gerade diese Pflanze dies nicht nur durch DMT alleine, sondern vor allem durch den Inhaltsstoff Bufotenin (5-Hydroxy-DMT) erhaelt. Cohoba ist staerker als DMT alleine! (eigen)
Jonathan Ott fuehrt ausserdem noch an, dass DMT chronisch genossen, sehr gefaehrlich ist und man auf jeden Fall nicht in der Lage ist ein Auto zu lenken. Ansonsten gelten nach Jonathan Ott die gleichen Grundregeln fuer den Konsum halluzinogener Drogen - man sollte niemals aengstlich, besorgt und uebermuedet in die Erfahrung gehen, in Ruecksicht auf die eigene Gesundheit, aber auch der Gesundheit der anderen, moeglicherweise Betroffenen Personen. Gleichsam ist eine ruhige und entspannende Umgebung grundsaetzlich Voraussetzung fuer jede Art von Konsum halluzinogener Drogen, nicht nur im Fall von DMT, um moegliche, sogar bleibende Schaeden, zu verhindern. (#62/190)
Der DMT-Rausch erfordert die volle Konzentration und Hingabe durch den Konsumenten und vertraegt sich ueberhaupt nicht mit dem Fuehren von Maschinen oder anderer Beschaeftigung, die ablenkt. Mit offenen Augen kann man zwar meistens die volle Kontrolle zurueckerhalten, doch die Wirkung ist so kurz bei DMT ohne MAO-Hemmer (DMT ist oral ohne MAO-Hemmung inaktiv, mit vorangehender MAO-Hemmung wird es aber oral wirksam und laenger), dass man auch keine Zeit fuer etwas anderes hat. (eigen)
Die Droge ist p.o. unwirksam (bis zu 1g gab es laut J. Otts Worten in seinem Werk "Pharmacotheon" keine Wirkung; (#45/137, #62/190)), da sie durch die Monoaminoxidase (MAO) abgebaut wird. Sie durchdringt damit nicht die Blut/Hirnschranke und gelangt somit nicht an ihren Wirkort im Gehirn. Erst durch Verwendung eines MAO-Hemmers kann die Substanz als Halluzinogen oral verwendet werden. (#32) J. Ott, Verfasser von "Pharamcotheon" stellte fest, dass die gleiche Dosis, wie bei einer i.m. Applikation oral verwendet werden kann, wenn die Monoaminoxidase ausreichend gehemmt wird. (#62/181)
Die Droge wurde medizinisch vor allem intramuskulaer verwendet. Es wurden dann 0,7-1,1mg/kg Koerpergewicht eingesetzt. (#12, #45, #57, #62) Diese Dosen erzeugen halluzinogene Wirkungen in 2-5 Minuten. Die Spitze der Wirkung wird in 15 Minuten erreicht und die ganze Erfahrung dauert 30-45 Minuten. (#62/181)
125mg DMT-Salz in 15ml, rektal verabreicht, waren ohne nennenswerte Wirkung, wie De Smet 1983 feststellte. (#62/181)
J. Ott fuehrt in seinem Werk "Pharmacotheon" Dosen von 25-30mg DMT-Freebase an - die die gleiche Wirkung haben, wie 50-60mg DMT-Salz i.m. Die Wirkung setzt jedoch im Gegensatz zur i.m. Applikation sofort ein, die Spitze ist nach 2-3 Minuten und die gesamte Wirkung ist nach 15-20 Minuten vorbei, wie Bigwood und Ott 1977 feststellten. (#62/181)
Jonathan Ott publizierte auch, dass 5-20mg DMT-Freebase intranasal keine Wirkung haben. Er stuetzte sich dabei auf die Untersuchungen von Turner und Merlis aus dem Jahr 1959. (#57)
Der Wirkungsbeginn ist bereits nach 3 Minuten. (#12, #36) Die Wirkungsdauer wird von Jonathan Ott mit nur 5-10 Min. angegeben, (#57) damit gehoert Dimethyltryptamin zu den kuerzesten wirksamen, halluzinogenen Rauschdrogen, die die Menschheit kennt. Dies ergibt sich vor allem daraus dass DMT eine endogene Verbindung im Gehin des Menschen ist, und von einem kooerpereigenen Enzym rasch metabolisiert wird. (eigen) Aeltere Quellen sprechen hingegen von 30-40 Minuten, in der die Wirkung anhaelt. (#12, #36) Bei ayahuaska ist die Dauer auf 3-4 Stunden ausgedehnt. (eigen)
Die Ausbildung einer psychischen Abhaengigkeit, wie bei LSD, wird von einer Reihe von Wissenschaftlern als moeglich erachtet. Doch wie bei LSD - ist die Bildung einer psychischen Abhaengigkeit auch hier stark umstritten - und derzeit nicht ausreichend belegt. Bei LSD muss man sogar - wo dieser Typ der "psychischen Abhaengigkeit" urspruenglich eingefuehrt worden ist, inzwischen davon ausgehen, dass genau das Gegenteil der Fall ist - der Konsum von LSD hoert bei einem sehr grossen Teil der Konsumenten (ueber 99%) nach einer gewissen Zeit (meist nach 2 - 3 Jahren) grundsaetzlich auf. Da der Begriff der "psychischen Abhaengigkeit vom LSD-Typ" sehr frueh und ohne gesicherte Erkenntnisse auf dieses halluzinogene Tryptamin uebertragen worden ist, muss man ebenso davon ausgehen, dass es keine ausreichenden Belege fuer die Bildung einer Abhaengigkeit gibt und diese Begriffsbildung aus Zeiten der fuercherlichsten Drogenprohibitionszeit stammt, wobei nicht einmal Beweise notwendig waren, um DMT als gefaehrlich einzustufen und es grundsaetzlich zu verdammen und zu verbieten sei, ohne dass es jemals ausreichende Untersuchungen an Menschen gegeben haette. Somit wurde wiederum ein altes, indigenes Rauschmittel, von der westlichen Industriegesellschaft verdammt, die im Gegensatz ihre eigenen eindeutig und bewiesenermassen gefaehrlichen Rauschmittel, v.a. den Alkohol, sogar noch medial bewirbt. Damit hat sich die repressive Drogenpolitik auf eine monopolistisch orientierte Wirtschaftspolitik reduziert. (eigen)
Da DMT in der westlichen Welt eine relativ seltene Droge ist und es ausserdem sehr kurz wirksam ist, gibt es in der Entgiftungspraxis von Aerzten kaum berichtete Vergiftungsfaelle. In diesem kurzen Wirkungszeitraum ist eben wenig Zeit vorhanden, dass sich grosse Probleme in der Psyche auftun und man noch einen Arzt mithineinzieht. Die Indianer des Amazonasgebietes kennen diese Problematik auf jeden Fall nicht, obwohl der Konsum dort gang und gaebe ist. (eigen)
Dennoch muss beachtet werden, dass auch DMT moeglicherweise in der Lage ist eine latent vorhandene schizophrene Psychose auszuloesen. Inwieweit sich Halluzinogene auf den Verlauf der als Schizophrenie bezeichneten Sammelkrankheit auswirken ist meines Wissens nicht ausreichend bekannt, noch wurde diese Problematik ausreichend untersucht. Tatsache ist es auf jeden Fall, dass es sehr wohl Menschen mit diagnostizierter Schizophrenie gibt, die Halluzinogene ohne Schaden konsumieren und andere, die davon sehr wohl stark negativ beeinflusst werden. Im negativen Fall treten meist Angstzustaende und Verstaerkung positiv-produktiver Symptome auf. Man kann davon sicherlich ableiten, dass bei den meisten Halluzinogenen sehr wohl eine partielle Beeinflussung des serotinergen (depressive Symptome) und dopaminergen (produktive Symptome, Angst) Systems stattfindet, doch ist die Erklaerung der Wirkungsweise von Halluzinogenen noch lange nicht genuegend geklaert. Aber auch die psychopharmakologische Beschaffenheit der Krankheit Schizophrenie ist in keiner Weise noch ausreichend erforscht. Die erforschte, psychopharmakologische Ebene und die subjektive Ebene des Erlebten (wie wir die Welt sehen und erleben, stimmungsmaessig und gefuehlsmaessig) klaffen noch weit auseinander. Grundsaetzlich muss auch noch von mir eingefuegt werden, dass man das menschliche Gehirn sicherlich als funktionelle Einheit betrachten muss, d.h. wenn man ein Teilsystem (bsp. dopaminerges System) irgendwie beschaedigt oder beeinflusst, es noch lange nicht erwiesen ist, dass damit ein Teilbereich des menschlichen Seins erkennbar gemacht wird. Man muss immer bedenken - dass das Nervenleitersystem ein komplexes Netzwerk ist und man wird nicht einen Teil alleine betrachten koennen. Es wird sicherlich noch Jahre, wenn nicht Jahrzehnte dauern, bis man in der Lage ist, Psychopharmakologie und Psychologie zu verbinden, denn ein Gespraech mit einer Person beeinflusst sicherlich X Systeme in unserem Gehirn, die allein nicht funktionell sind. Dennoch ist es durch Einsatz von Medikamenten, Halluzinogenen und anderen Techniken gelungen kleine Teile des Gesamten zu verstehen und bestimmte gefuehlsmaessige,Wahrnehmungs- oder kognitive Funktionen zu veraendern und dadurch Aufschluss ueber die Wirkungsweise eines Teils des Ganzen zu gewinnen. So hat die Halluzinogenforschung, oder auch die Opiatforschung sehr wohl zu einem tieferen Verstaendnis der Funktion des Erlebens gefuehrt, doch kann man das menschliche Sein immer noch nicht auf der chemischen Ebene ausreichend verstehen. Dennoch wird es notwendig sein in diesem Bereich weiterzuforschen - auch im Bereich der Halluzinogene - denn diese Substanzen haben eine ausgesprochene Wirkung auf unser Wahrnehmen, vor allem auf das visuelle und auditive Wahrnehmen. Auch die Erforschung antagonistisch wirksamer Substanzen, wie zum Beispiel von d2- oder 5-HT-2A/2C-Hemmern oder anderen psychoaktiv wirksamen Mitteln, kann bereits einen Teilmechanismus aufdecken. Halluzinogene als visuell-produktive "Medikamente" koennen den Farbensinn veraendern und haben bereits bei veranlagten Menschen erwiesenermassen nach der halluzinogenen Erfahrung, eine Beeinflussung ihrer Schoepfungskraft erbracht. Man muss sich immer wieder der Erlebnisse von A. Huxley, von E. Juenger und anderen Groessen erinnern, die Nutzen aus den "produktiven" Symptomen gezogen haben. Auch beruehren halluzinogene Erfahrungen einen Bereich - den die meisten Menschen in das Religioese einordnen und loesen Symptome aus, die von den einen als Wahnsinn, den anderen als religioese Erfahrung betrachtet werden, denn vieles was wir noch nicht erklaeren koennen, wird meist dem Goettlichen oder Teuflischen zugeordnet. Begriffen des Nichtverstehens, meines Erachtens. So war es in der bekannten Geschichte. Ein Schuss aus einer Waffe, den Pizarros Moerdertruppen in Amerika losloesten - ist fuer die dortigen Ureinwohner als etwas unverstaendliches erlebt worden und sofort dem Goettlichen zugerechnet worden, was sich spaeter in der Zerstoerung ihrer Kultur geraecht hat, denn Ihr Vertrauen in die goettliche Ueberlegenheit der Spanier wurde von diesem masslos ausgenutzt. (eigen)
Sollte es dennoch zu Problemen bei der Einnahme von DMT kommen, muss bedacht werden, dass die Wirkung sowieso in wenigen Minuten aufhoert und es meist nicht notwendig ist weitere Massnahmen, wie die Verabreichung von Beruhigungsmitteln, durchzufuehren. Auf jeden Fall sollte bei bleibenden psychotischen Symptomen ein Vertrauensarzt aufgesucht werden, mit dem man dann entscheiden kann, ob der Einsatz von Neuroleptika u.U. geeignet ist, um positiv-produktive Symptome zu unterdruecken. (eigen)
Rauchen der Reinkristalle (der Freebase!) in der Purpfeife:
Die Kristalle werden vorsichtig erhitzt, bis sie langsam schmelzen und verdampfen. Die entstehenden Daempfe werden inhaliert. (eigen)
Rauchen der Substanz (Freebase) vermengt mit anderen Pflanzen:
Die Substanz (die Freebase!) wird in einem Loesungsmittel geloest (am besten Wundbenzin) und anschliessend auf eine Traegersubstanz aufgebracht. Hierzu dienen Petersiel, Damiana, Tabak, Minze, Katzenminze,...). Die eingetrockneten, inzwischen auch kaeuflich erwerbbaren Rauchmischungen, werden dann entweder in einer Pfeife oder in einem Joint geraucht. Ein Grund fuer diese Bereitung ist der sattsam, fuerchterliche Plastik-Geschmack von gerauchten DMT, der damit uebertuencht werden soll, (#62/190f.) was unmoeglich ist, und die Unverfaelschbarkeit des Materials aufzeigt. DMT-Freebaserauchen ist extrem hart fuer die Lunge und schaedlich. Bei Pflanzenbasierenden Rauchmischungen ist zu beachten, dass DMT erst am Schluss des Pyrolyse-vorgangs verdampft, und so die gesamte Rauchmischung bis zum bitteren Ende geraucht werden muss. (eigen)
Rauchen mittels eines Vaporizers/Verdunsters
Es gibt eine Reihe verschiedenartiger Geraetschaften zur Verdampfung/Verdunstung von Inhalationsmaterial, dass verwendet werden kann. Aufpassen muss man auf den niederen Siede- und Zersetzpunktes von DMT, der vielfach schon erreicht ist und wie beim Rauchen mit Pflanzenmaterial oder Purbaserauchen, die fehlende Effizienz der Verfahrens aufzeigt. (eigen)
Oraler Konsum mittels MAO-Hemmer:
Damit die oral unwirksame Rauschdroge DMT oral aufgenommen werden kann, ist eine ausreichende Hemmung des koerpereigenen Enzyms MAO (Mono-Amin-Oxidase) notwenig. Dieses Prinzip wurde uebrigens schon vor Jahrhunderten am Amazonas, von dort lebenden Indianern, entwickelt. (#57, #62)
"Fixen":
DMT wurde bei den wenigen klinischen Untersuchungen, die es gab, meisten i.m. injeziert. (#12, #45, #57, #62)
"Rektal":
Unwirksam - scheint derzeit der Konsens zu sein, doch die vorliegenden Materialien sind nicht genau genug niedergeschrieben, dass man alle Applikationsparameter, wie Dosis, Freebase/Salz-form, Einnahmeverlauf entnehmen oennte. (eigen)
Grundsaetzlich gibt es 2 verschiedene Verfahren um DMT aus Pflanzen, oder aehnlichem, zu extrahieren:
Zuerst wird mit verd. Saeure ein waessriger Alkaloidauszug erstellt, mit einem nicht-polaren Loesungsmittel (Wundbenzin) entfettet, dann wird die Base mit einer Lauge free-gebased. Jetzt kann es schon verwenden oder weiter reinigen, oder ein Salz bereiten,....Jede DMT-haeltige Pflanze ist geeignet. Weiterverarbeitung gleich wie unten. (eigen)
Es wird direkt NaOH zum Pflanzenmaterial gefuegt, man laesst es einige Zeit ziehen, und extrahiert das Freebase DMT mit Wundbenzin oder einem aehnlichen non-polaren Loesungsmittel (NaOH und Wundbenzin sind der derzeitige Standard).
Urspruenglich gezeigt fuer die alkaloidreiche Mimosa hostilis Wurzelrinde. Entweder weiter reinigen, gebrauchen (rauchen oder oral mit MAO Hemmer) oder Salzfaellen. Grundsaetzlich laesst sich dieses Verfahren auch auf jede andere DMT-haeltige Pflanze uebertragen, Ausbeute je nach Gehalt, div. andere Pflanzen wurden von uns getestet (s. Psychotria viridis Diplopterys cabrerana,...). (eigen)
Einsatz von Ca(OH)2 als Laugenersatz fuer die NaOH, notfalls CaO oder Na2CO3 als basisches Salz, fuer die Aufschliessung des Alkaloids. Theoretisch aufgearbeitet und uebersetzt bei Anadenanthera-Arten, dzt. noch nicht ausreichend getestet. Aceton und Zitronensaeure sind eine weiterer Ansatz, der moeglich ist.(eigen)
Michael Valentine Smith gibt in seinem Werk "Psychedelic Chemistry", dass lange Zeit als Zusammenfassung bestehender wissenschaftlicher Literatur in diesem Bereich der Drogenforschung gedient hat, folgendes Verfahren an, dass eigentlich zur Herstellung von DET geeignet ist, aber bei entsprechender Veraenderung auch fuer die Synthese von DMT geeignet ist: Doch es spricht einiges gegen diese Beschreibung, denn sie ist viel zu wenig praezise:
5,5g Indol, 15ml Cyclohexan und 0,5g pulversiertes Kupfer werden zusammengefuegt. Es wird am Rueckfluss gekocht und tropfenweise 2,9g Diazoazeton dazugefuegt. Nach einer bestimmten Zeit laeuft die Reaktion schnell ab und bildet 2 Schichten aus. Der ueberschuessigen Kupferkatalysator wir entfernt, indem man filtriert. Es wird anschliessend unter Vakuum verdunstet oder destilliert, um 2,6g 3-Indolyl-aceton zu bekommen.
3,3g 3-Indolyl-aceton in 100ml EtOH; Es wird ueber einen Palladium-Carbon Katalysator in Gegenwart von 0,04M MEA reduziert. Nach 2h wird filtriert und unter Vakuum verdunstet, um DET zu erhalten. (#23)
Diese Quelle wurde dem Internet entnommen und es fehlt derzeit noch eine Bestaetigung durch eine gedruckte Quelle:
Es wird ein 1l Rundbodenkolben unter einem Abzug in ein Eisbad platziert. Es werden 400ml kalter, wasserfreier Aether in den Kolben gegeben, in dem dann 60g Indol unter Ruehren geloest werden. Zu 100ml wasserfreien Aether in einem Scheidetrichter werden 50g Oxalylchlorid hinzugefuegt. Diese Loesung wird langsam in die kraeftig geruehrte Indol-loesung getropft, verteilt auf eine Dauer von 10-15 Min. Das Ruehren wird 10 Min. laenger fortgesetzt. Man laesst den Niederschlag ein paar Minuten absetzen und dann wird die Fluessigkeit dekantiert. Es wird wasserfreier Aether hinzugefuegt und gut durchgemischt. Es wird gewartet, bis sich die Reaktionsloesung abgesetzt hat. Dann wird die Fluessigkeit wieder dekantiert. Wenn die Reinheit des Niederschlags zufriedenstellend ist, belaesst man den goldenen Niederschlag im Kolben fuer den naechsten Schritt, der sofort folgen muss. Die Ausbeute betraegt annaehernd 100g.
Dimethylamin reagiert sofort mit Indoloxalylchlorid. Es werden rund 400ml eiskalter, wasserfreier Aether zum gleichen 2-Hals 1l Rundbodenkolben, der im ersten Schritt benutzt worden ist, in dem sich auch der gleiche Niederschlag aus dem Syntheseschritt I befindet, zugefuegt. Das Eisbad wird weiter durch Gebrauch von Salz und Eis abgekuehlt. Das Gewicht des Niederschlags wird geschaetzt und 100g Indoloxalylchlorid (IOC) werden verwendet. Fuer dieses Gewicht an IOC werden noch versiegelte Behaelter mit Dimethylamin (DMA) verwendet, weil es nicht haltbar ist, wenn das Containersiegel aufgebrochen ist und Frischluft hinzutritt. Das Dimethylamin im Behaelter wird merklich unter 0 Grad Celsius abgekuehlt und 1 Teil Amin wird in 3 Teilen wasserfreiem, kalten Aether geloest. (Amine koennen in dieser Loesung gelagert werden.) Die Vorratsloesung wird fuer den Gebrauch auf Zimmertemperatur erwaermt und es wird die entsprechende Menge verwendet. Es wird die gleiche Apparatur verwendet, wie beim Zufuegen des Oxalylchlorids. Die Aminloesung wird langsam zum IOC mit kraeftigem Ruehren zugefuegt. Es wird 0,5h lang geruehrt. Nachdem die Addition fertig ist, laesst man die Temperatur steigen. Der Niederschlag wird im Vakuum filtiert, mit Aether gewaschen, gefolgt von einer Waschung mit Aether/H2O. Es ist besser, die Aether-H2O Loesung mit dem Niederschlag vor der Filtration aufzuschuetteln. Umkristallisieren aus heissem EtOH oder aus einer 1:1 MeOH-Benzol-mischung.
Das Indolglycoxalamid wird durch Schmelzsublimation bereitet und in kleine Stueckchen zerkleinert, wenn Aether als Loesungsmittel genutzt wird. Die Aluminiumfolie erzeugt einen gute Masse giessbereiter Stuecke, welche durch den Kuehler passen muessen. Ebenso kann ein Soxhletextraktor benutzt werden, um die Kristalle durch langsames Loesen in den Aether hinzuzubringen. THF, wenn vorhanden, loest IGA und die Verbindung wird langsam in Loesungsform hinzugefuegt.
Zu einer geruehrten Mischung von 15g LAH in 300ml wasserfreiem Aether (oder THF) fuege langsam die Stuecke (oder Loesung) von IGA zu, bis 20g Gesamtmenge zugefuegt worden sind. Halte die Reaktionsrate auf einen kontrollierbaren Level, es koennte sonst ueberkochen! Ruehre und koche am Rueckfluss fuer 90 Minuten, nachdem die Addition komplett ist. Kuehle in einem Eisbad ab und beginne vorsichtig den Komplex mit Eisstuecken oder einer kalten MeOH-Loesung zu hydrolysieren, die durch den Kuehler zugefuegt werden. Wenn es keine weitere Reaktion mehr gibt, fuege wenige ml Wasser hinzu und lass es ein paar Stunden ruhen, mit gelegentlichem Herummschwappen der Inhaltsstoffe. Lass alles schliesslich absitzen und dekantiere die klare Fluessigkeit in einen Verdunstungskessel. Filtriere den Rest und wasche einige Male mit Aether-MeOH oder THF-MeOH. Verdampfe die vereinten Extrakte und wenn noetig, besame den schweren Sirup mit Kristallen aus DMT. Ohne Samenkristalle braucht das Produkt Tage oder gar Wochen zum Kristallisieren. Dieses Rohprodukt ist zum Rauchen geeignet. Um das DMT zu reinigen, beginne, nachdem das LAH mit MeOH zersetzt worden ist. Fuege 500ml gesaettigte Na2SO4 Loesung hinzu, mische und filtriere. Wasche mit Aether oder THF. Neutralisiere das Filtrat mit 0.1N HCl. Extrahiere mit Aether. Neutralisiere die untere Schicht mit 0.1N NaOH. Extrahiere diese Loesung sofort mit CHCl3. Die Chloroformschicht wird ueber wasserfreiem Na2SO4 getrocknet, konzentriert, und aus ihr kristallisierte DMT bei der Zugabe von Petrolaether. Die Mutterfluessigkeit kann chromatographiert werden mit einer Tonerdesaeule, und Benzol-MeOH im Verhaeltnis 99.8:0.2 enthaelt. (USENET - Quelle muss ausgetauscht werden durch Originalarbeit!!!)
Von Alexander Shulgin stammt aus seinem Buch Tihkal jene Beschreibungen der Synthese von DMT:
(von N,N,N-Trimethyltryptammoniumiodid, Dimethyltryptaminmethiodid, DMT-CH3I): Dieses quartaere Salz wird von Tryptamin und Methyljodid bereitet. Zu einer geruehrten Loesung von 3 g Tryptamin in 30 mL IPA wurde 10 g Methyliodid hinzugefuegt. Creme-farbene Feststoffe erschienen sofort und nach 12 h Ruehren bei Zimmertemperatur wurden diese durch Filtration entfernt, zweimal mit IPA und warmen IPA gewaschen, und an der Luft getrocknet zu konstantem Gewicht. Es wurden so 1.81 g N,N,N-Trimethyltryptammoniumiodid erhalten. Umkristallisation eines analytischen Beispiels, Acetonnitril gebrauchend, ergab ein weisses kristallines Produkt mit einem Schmelzpunkt von 210-211 Grad Celsius. Im Prinzip, DMT wurde im Filtrat zusammen mit NMT und Tryptamin selbst erhalten. Das Tryptamin kann entfernt werden aufgrund seiner Aetherloeslichkeit und das NMT durch seine Umwandlung zum Benzamid mit Essigsaeureanhydrid oder Benzoylchlorid. Das verbleibende Grundmaterial ist hauptsaechlich DMT, welches weiter gereinigt werden kann als Pikratsalz. Die Ausbeute ist gering, und bessere Ergebenisse werden durch die Demethylation dieses Salzes erhalten.
Die Demethylation des Iodidsalzes: Unter einer Inertatmosphaere wurde eine Loesung von 0.40 g N,N,N-Trimethyltryptammoniumiodid in 5 mL THF versetzt mit 1.5 mL 1M LiEt3BH in THF und wurde am Kochen am Rueckfluss 9 h lang gehalten. Nach dem Abkuehlen wurde die Mischung angesaeuert mit verduennter HCl und das THF wurde im Vakuum entfernt. Der Rest wurde suspensiert in verduennter NaOH und mit Et2O extrahiert. Die Extrakte wurden vereint, und das Loesungsmittel wurde im Vakuum entfernt, um einen Rest von 0.12 g N,N-Dimethyltryptamin (DMT) als kristallinen Feststoff mit einem Schmelzpunkt von 57-59 Grad Celsius zu erhalten.
Die Demethylation des Chloridsalzes: Eine heisse waessrige Loesung von N,N,N-Trimethyltryptammoniumiodid wurde versetzt mit einem Ueberschuss an frisch niedergeschlagenen AgCl, und alles wurde sanft 15 Min. lang gekocht. Die gemischten Silberhaliden wurden durch Filtration entfernt, und das Filtrat wurde befreit von H2O so schnell es ging. Zu dem Rest wurde hinzugefuegt eine kleine Menge an MeOH gefolgt von Aceton bis die Kristallisation von N,N,N-Trimethyltryptammoniumchlorid fertig war. Es hatte einen Schmelzpunkt von 193 Grad CelsiusC (80%), und es ist betraechtlich mehr wasserloeslich, als das Startmaterial. Dieses Salz wurde pyrolisiert, und unter hartem Vakuum wurde der Rest wurde destilliert. Das Destillat wurde geloest in einer kleinen Menge Methanol und angesaeuert mit verduennter Salpetersaeure. Eine kleine Menge des unloeslichen Materials wurde durch Filtraton entfernt, die waessrige Phase mit CHCl3 gewaschen, basisch gemacht mit waessriger NaOH, und mit CHCl3 extrahiert. Das Loesungsmittel wurde im Vakuum entfernt, und der Rest wurde versetzt mit einer Loesung von Pikrinsaeure. Dies wurde dekantiert von ein wenig unloeslichem Material, und langsam abgekuehlt, um das Pikratsalz von DMT als gelbe Nadeln mit einem Schmelzpunkt von 167 Grad Celsius Celsius zu ergeben. Eine waessrige Suspension von diesem Pikrat wurde basisch gemacht mit einem Ueberschuss an waessriger NaOH, mit Et2O extrahiert, und das Loesungsmittel wurde im Vakuum entfernt, um einen blass gelben Rest zu ergeben, der kristallisierte. Dieser wurde auf eine poroese Platte gepresst und mit Petrolaether gewaschen, um N,N-Dimethyltryptamine (DMT) als blass weissen Feststoff mit einem Schmelzpunkt von 47 Grad Celsius zu ergeben.
Die Demethylation des Thiophenolatsalzes: Eine Suspension von 2.5 g N,N,N-Trimethyltryptammoniumiodid in 25 mL MeOH wurde gebracht in Loesung durch Erhitzen, und mit 1.0 g Ag2O versetzt. Die Mischung wurde erhitzt fuer 10 Min. auf dem Dampfbad, die Feststoffe werden durch Filtration entfernt und mit zusaetzlichen 20 mL MeOH gewaschen. Die Methanolloesungen wurden mit 1.0 g Thiophenol versetzt und das Loesungsmittel wurde im Vakuum entfernt. Das resultierende zaehfluessige Oel (2.12 g) wurde mit einer Flamme erhitzt zum Kochen am Rueckfluss und es gab ausgepraegte Blasenbildung. Nach 5 Min. wurde die hellfarbene Reaktionsmischung abgekuehlt auf Raumtemperatur, in 50 mL CH2Cl2 geloest, und mit zwei 25 mL Portionen verduennter HCl extrahiert. Diese wurden vereint (blass gelbe Farbe), mit 5%-iger waessriger NaOH basisch gemacht und mit 3x25 mL CH2Cl2 extrahiert. Nach dem Entfernen des Loesungsmittels von den vereinten Extrakten, wurde der Rest (ein bernsteinfarbenes Oel, 1.04 g) mit einem Kugelrohrapparat destilliert. Ein weisses Oel destillierte ueber bei 130-140 Grad Celsius mit einem Druck von 0.1 mm/Hg, und kristallisierte ploetzlich. Dieses Destillat wog 0.77 g, und wurde aus siedendem Hexan umkristallisiert, nach dem Dekantieren der Loesung von einer kleinen Menge an unloeslichen Stoffen. Es wurden so 0.40 g Dimethyltryptamin (DMT) mit einem Schmelzpunkt von 67-68 Grad Celsius Celsius erhalten. Das Destillat beinhaltete rund 3% 2-Methyl-1,2,3,4-tetrahydro-beta-carbolin als Verunreinigung, die beim Umkristallisieren verloren ging.
(von Tryptamin und Ethylformat aus)
Eine Suspension von 1.0 g Tryptamin in 50 mL Ethylformat wurde am Kochen am Rueckfluss 15 h lang gehalten, waehrend dieser Zeit wurde die Mischung homogen. Die fluechtigen Stoffe wurden im Vakuum entfernt, um zu den oeligen Rest des Formamids zu ergeben. Dies kann durch Destillation gereinigt werden, doch das ungereinigte Produkt kann ausreichend befriedigend im naechsten Reaktionsschritt verwendet werden. Dieser Rest wurde in 50 mL wasserfreiem THF geloest und tropfenweise zu einer Loesung von 1.0 M LAH in THF (40 mL, 40 mmol) hinzugefuegt, welche verduennt mit anderen 50 mL THF worden war. Nachdem die Addition fertig war, wurde die Reaktionsmischung unter Rueckflusskochbedingungen 15h lang erhitzt. Das Kochen am Rueckfluss wurde fortgesetzt, als eine Loesung von 40 mL 1.0 M frisch destilliertem Ethylformate in THF tropfenweise ueber die Dauer von 2h hinzugefuegt wurde. Das Erhitzen wurde abgebrochen und die Reaktionmischung wurde unterbrochen durch die Addition von ueberschuessigen, festen Natriumsulfatdecahydrat bei Raumtemperatur. Die Reaktionmischung wurde filtriert und die Filtrate wurde im Vakuum konzentriert um 1.15 g reines N,N-Dimethyltryptamin als ein Oel zu ergeben, dass sich verfestigte beim Stehen im Gefrierschrank. Das Material kann umkristallisiert werden aus Hexan, um weisse Kristalle mit einem Schmelzpunkt von 67 Grad Celsius zu ergeben.
(von Indol aus) Zu einer gut geruehrten Loesung von 10 g Indol in 150 mL wasserfreiem Et2O wurde tropfenweise ueber die Dauer von 30 Min. eine Loesung von 11 g Oxalylchlorid in 150 mL wasserfreiem Et2O hinzugefuegt. Das Ruehren wurde fuer zusaetzliche 15 Min. fortgesetzt, waehrend dieser Zeit gab es die Bildung von Indol-3-ylglyoxylchlorid als einen gelben, kristallinen Feststoff. Dieses Zwischenprodukt wurde durch Filtration entfernt und mit Et2O gewaschen. Es zerfiel mit einer bedeutenden Rate bei Zimmertemperatur, und sollte gebraucht werden, so schnell wie moeglich nach der Bereitung. Der Diethylaether in dieser Synthese kann vorteilshafterweise ersetzt werden mit t-butylmethylaether (TBME), was ebenso gut als Loesungsmittel in dieser Reaktion arbeitet, aber die potentiellen Gefahren der Peroxidbildung vermeidet. Das obige Indol-3-ylglyoxylchlorid wurde zu 20 g wasserfreien Dimethylamin in 150 mL kaltem, geruehrten und wasserfreiem Et2O hinzugefuegt. Wenn die Farbe grossteils verschwunden worden war, wurde ein Ueberschuss an 2N HCl hinzugefuegt, die Mischung wurde abgekuehlt, und die resultierenden Feststoffe wurden durch Filtration entfernt. Diese wurden aus EtOAc umkristallisiert, um nach Lufttrocknen 14.6 g (79%) Indol-3-yl-N,N-dimethylglyoxylamid mit einem Schmelzpunkt von 159-161 Grad Celsius zu ergeben.
Eine Loesung von 14 g Indol-3-yl-N,N-dimethylglyoxylamid in 350 mL wasserfreiem THF langsam hinzugefuegt zu 19 g LAH in 350 mL THF, welche gut geruehrt wurde und am Kochen am Rueckfluss unter einer Inertatmosphaere gehalten wurde. Nachdem die Addition fertig war, wurde das Kochen am Rueckfluss aufrechterhalten fuer zusaetzliche 16 h, die Reaktionmischung wurde abgekuehlt, und das ueberschuessige Hydrid wurde durch die vorsichtige Addition von nassem Dioxan zerstoert. Die gebildeten Feststoffe wurden durch Filtration entfernt, mit heissem THF gewaschen, die Filtrate und Waschungen wurden vereint, ueber wasserfreiem MgSO4 getrocknet, und das Loesungsmittel wurde im Vakuum entfernt. Der Rest wurde geloest in heissem Petrolaether. Beim Abkuehlen bildeten sich Kristalle aus N,N-Dimethyltryptamin (DMT), die frei vom Loesungsmittel filtriert worden waren und an der Luft getrocknet wurden, und 11.1 g (91%) wogen. Es gab Berichte von Nebenprodukten von dieser LAH Prozedur, wenn sie in Et2O durchgefuehrt wird, die die Reinheit des Endprodukts schaedigen. Um das HCl Salz von DMT zu erhalten, wurde der Rest geloest in wasserfreiem Et2O und gesaettigt mit wasserfreiem HCl. Die resultierenden Kristalle wurden aus Benzol/Methanol umkristallisiert, um N,N-Dimethyltryptaminhydrochlorid mit einem Schmelzpunkt von 165-167 Grad Celsius zu ergeben. Die Ausbeute von 14 g des Amins waren 13.3 g des Salzes. (#101/412ff.)
800 n. Chr.: Grabstaetten in Nordchile beinhalten Taschen mit Schnupfuntensilien, Reste von Schnupfpulvern die DMT, 5-Methoxy-DMT und Bufotenin beinhalten. Andere Graeber enthalten Samen von Anadenanthera ssp. (Tryptamine Palace)
1496: Bruder Friar Ramon Pane dokumentierte ein Schnupfpulver mit dem Namen cohoba/yopo unter den Taino, diet heute ueberein dass cohoba/yopo sicherlich aus Anadenanthera peregrina gemacht worden ist und DMT, 5-Methoxy-DMT und Bufotenin beinhaltete. (Tryptamine Palace)
16.-19. Jhdt.: Cohoha Schnupfpulver vom yopo-Baum wird von den Eingeborenen Kolumbiens und angrenzender Gebiete gebraucht. (Tryptamine Palace)
1560: Indianer entlang des Rio Guaviare in Kolumbien nehmen yopo mit Tabak (Nicotiana tabacum). (Tryptamine Palace)
1571: Indianische Medizinmaenner machen Prophezeihungen durch Berauschung, erzeugt durch das Trinken von vilca, einer DMT beinhaltendem Bereitung von Anadenanthera colubrina. (Tryptamine Palace)
1741: Ein Jesuit schrieb ueber den cohoba-Gebrauch bei den Einheimischen in Kolumbien und Venezuela. (Trytamine Palace)
1801: Baron Alexander von Humboldt identifizierte den yopo-Baum als Anadenanthera peregrina. (Tryptamine Palace)
1931: In diesem Jahr erfolgte erstmals die Synthese der halluzinogenen Rauschdroge durch Richard Manske. (#62/433, #45/134) Die Wirksamkeit des Molekuels war noch nicht bekannt und so wurde es gleich ad acta gelegt. (Tryptamine Palace)
1939: Virola-Genus identifiziert als Quelle von einem Schnupfpulver namens epena im kolubianischen Amazonasgebiet, Venezuelas und Westbrasiliens. (Tryptamine Palace)
1954: Eine weitere Synthese von DMT durch Speeter wurde entwickelt. (#62/433, #45/136)
1946: Oswaldo Goncalves de Lima isolierte als Erster DMT, welches er Nigerin nannte, aus jurema preta Mimosa hostilis (= M. teniflora) (er publizierete in span.). J. Ott berichtete, dass Nigerin eine unreine Form von DMT war. (Tryptamine Palace)
1953: W. Burroughs reiste durch Kolumbien und Peru auf der Suche nach yage. (Tryptamine Palace)
1955: Es erfolgte die Isolation durch die Arbeitsgruppe Fish, Johnson und Horning aus den Samen von Anandenanthera peregrina, einer schon seit Jahrhunderten als Halluzinogen verwendeten Pflanze der Neuen Welt. (#62/163, #45/136)
1956: Stephen Szara und Freunde waren in Ungarn die ersten, welche die Reinsubstanz DMT in der Form des Hydrochlorids testeten. (#62/163) Er stellte die orale Unwirksamkeit des DMT fest und fuehrte sie auf ein neutralisierendes Prinzip im Magen-Darm-Trakt zurueck. Er injizierte selbst synthetisiertes DMT und entdeckte damit die halluzinogene Wirksamkeit von DMT. Spaeter fluechtte er aus Ungarn mit seinem DMT und emigrierte in die USA, wo er bis zu seinem Rueckzug in 1981 beim National Institute of Health in Betsethba, Maryland, arbeitete. Er war auch Direktor des Preclinical Research at the National Institute on Drug Abuse fuer viele Jahre. (Tryptamine Palace) Die Arbeit lautete auf: St. Szára, Experientia 12, 441 (1956); (MerckIndex)
1957: DMT-Isolation aus den Bleaettern von Prestonia amazonica (Benth.) Macbride (Haemadictyon amazonicum Spruce & Benth.), Apocynaceae: Hockstein, Paradies, J. Am. Chem. Soc. 79, 5735 (1957). (MerckIndex)
1957: Arnold und Hofmann beschaeftigten sich ebenfalls sehr frueh mit DMT und publizierten ueber diese Verbindung. (#45/137)
1958: Sai-Halas-z et al. publizierten ebenso ueber DMT. (#45/137)
1959: Die Studien ueber DMT wurden spaeter von Turner und Merlis bestaetigt. (#45/137)
1959: DMT ist unzweifelhaft in Mimosa tenuiflora enthalten, wurde festgestellt, nachdem Goncalves amerikan. Chemiker mit den Wurzeln dieser Pflanze versorgte. (Tryptamine Palace)
1959: Dr. Oscar Janiger war die erste Person in der USA, der eine klinische Untersuchung des Halluzinogens DMT mit Menschen durchfuehrte. Er injizierte sich selbst DMT und erlebte das volle Spektrum der Wirkungen. Er hat sich eine eigene Versorgung mit DMT synthetisiert, als er beim Lesen einer Arbeit uber Ayahuasca die Aehnlichkeit von DMT und Gehirnneurotransmittern entdeckte. Er gab das DMT an Alan Watts und Captain Al Hubbard zur Verteilung in die aufstrebende psychedelische Gemeinde an der Westkueste. Der Konsenz war, dass es eine hoellische halbe Stunde war, ohne Erholungswert. (#46)
1961: Der amerikanische Schriftsteller und Drogenkonsument William Burroughs, (#62/164) bekannt fuer seine Romane "Junkie" oder "Naked Lunch", der letztere wurde auch in hervorragender Weise verfilmt, (eigen) begann seine ersten Selbstexperimente mit dem Halluzinogen DMT in diesem Jahr. Er probierte verschiedene Dosen im Bereich von 65mg - bis er eine Dosis von 100 mg einnahm, die eine fuerchterliche Erfahrung fuer ihn darstellte und er als Ueberdosis empfand. (#62/164) Burroughs publizierte auch ein Buch "Auf der Suche nach Yage.", welches seine Erfahrungen mit diesem Mittel zusammenfasste. (eigen)
1963: In Anbetracht der Warnungen von William Burroughs probierten Timothy Leary und Ralph Metzner an der Harvard Universitaet das Halluzinogen in einer eigens bereiteten Umgebung. Ralph Metzner berichtete in diesem Jahr in seinem Buch "The Psychedelic Review", dass DMT in Dosen von 1mg/kg gleich wie LSD oder Meskalin wirke, aber mit einer viel kuerzeren Wirkdauer. (#62/164)
1964: DMT wird in der Einfuehrung der "Psychedelic Experience" von T. Leary, R. Matzner und R. Alpert erwaehnt. (Tryptamine Palace)
1965: Snyder und Merril untersuchten Beziehungen zwischen der halluzinogenen Aktivitaet und der elektronischen Struktur der Verbindung. Snyder, Merril, Proc. Nat. Acad. Sci. USA 54, 258 (1965). (MerckIndex)
1965: 5-Methoxy-DMT wurde in Bufo alvarius entdeckt. (Tryptamine Palace)
1966: DMT wurde in diesem Jahr illegal gemacht! (Tryptamine Palace)
ca. 1965-66: Nicholas Sand, Untergrundchemiker bekannt fuer Orange Sunshine LSD, entdeckte die Rauchbarkeit von DMT-freebase oder -fumarat. (Tryptamine Palace)
1965: Ein deutsches Team isolierte DMT aus menschlichen Blut. (Tryptamine Palace)
1967: Er erschien eine Arbeit zum Thema Metabolismus von DMT von B. R. Sitaram et al., Biochem. Pharmacol. 36, 1509 (1987). (MerckIndex)
1968, Holmstedt, Lindgren, und Agurell vermuteten zuerst, dass die Wirkungen von ayahuasca verursacht werden durch eine Kombination von natuerlich vorkommenden Monoaminxidasehemmern und DMT. (Tryptamine Palace)
Maerz 1968: Das DEA berichtet im Journal microgram, dass DMT auf den Strassen erhaeltlich ist, beides als Pulver und impraegniert auf Marijuana und Tee. (Tryptamine Palace)
1969: In diesem Jahr erfolgte eine Isolation von DMT durch Agurell aus Virola theiodora, einer in Suedamerika als Quelle eines halluzinogenen Schnupfpulvers bekannten Pflanze. Damit wurde das Wirkprinzip des epena genannten Schnupfpulvers erkannt und auf die Wirkung von DMT und des nahe verwandten 5-Methoxy-DMTs zurueckgefuehrt. (#62)
1970, der amerikanische Kongress befuerwortete die Scheduling Laws, die es fast ganz unmoeglich machten. irgendeine Forschung mit LSD, Meskalin oder DMT zu betreiben. Dies stoppte die wissenschaftliche Untersuchung dieser Verbindung in den USA. (Tryptamine Palace)
1970: Die erste Identifikation von anderen DMT-haeltigen Pflanzen, die Psychotria viridis, wurde vom Team um den amerikan. Forscher A. Der Marderosian durchgefuehrt. Nicht nur entdeckten sie in den Blaettern dieser Art von den Cashinuaua-Indianern DMT, sondern sie waren auch die ersten, die es in einem Dekokt namens ayahuasca entdeckten, bereitet von den Indianern. (Tryptamine Palace)
Das Halluzinogen in seiner Reinform spielte niemals eine grosse Rolle als verbreitete Strassendroge noch als rituelles oder hedonistisches Halluzinogen in der westlichen Welt. (#62/164)
1971: Durch die Psychotropenverordnung der "single-convention on narcotis drugs" wird DMT als "Narkotika" von der UNO verboten. (eigen)
1972: Julius Axelrod entdeckte DMT im menschlichen Gehingewebe, einen Schritt weiter darauf im menschlichen Urin und in der Cereborspinalen Fluessigkeit, in der das Gehin badet. DMT war damit das erste endogene Halluzinogen, das gefunden wurde, spaeter (1975) kam das nahe verwandte 5-Methoxy-DMT hinzu durch die Arbeiten von S.T. Christian. (Tryptamine Palace)
1976: "The invisible Landscape" von T. und D. McKenna wurde publiziert. (Tryptamine Palace)
1970: Eine Synthese fuer DMT wurde veroeffentlicht: I. Fleming, M. Woolias, J. Chem. Soc. Perkins Trans. I 1979, 829. (MerckIndex)
1981: Eine Ueberblicksarbeit ueber die Biosynthese, den Metabolismus und die Bioaktivitaet wurde veroeffentlich: S. A. Barker et al., Int. Rev. Neurobiol. 22, 83-110 (1981). (MerckIndex)
Spaete 1980'er: Es kommt langsam zu einer Verbreitung der Rauschdroge ayahuaska und in diesem Zusammenhang auch zu einer Verbreitung von DMT. Ayahuaska-zeremonien werden inzwischen in Suedamerika an Touristen allgemein verkauft, gleich Haschisch in Indien. Aber auch in Amsterdam und anderen europaeischen Grossstaedten werden ayahuaska-Rituale, die ja auf einer Mischung von beta-Karbolinenen und DMT beruhen, kaeuflich angeboten. In Brasilien haben sich eigene Religionen, um den Gebrauch von ayahuaska formiert, der sogenannte Santo Daime-Kult, oder auch die Unio de Vegetal. (eigen)
1985: Der fluorometrische Nachweis von DMT wurde veroeffentlicht: O. Jules et al., Anal. Chim. Acta 169, 355 (1985). (MerckIndex)
1991: 250 Leute in San Francisco gehen zur Black Rock Wueste in Nevada, um einen hoelzernen Mann zu verbrennen, erzeugt von Larry Harvey. Idee des Burning-man festivals! (Trptamine Palace)
1991: Verschiedene Wechselwirkungen von DMT mit Serotoninrezeptor-subtypem wurden untersucht: A. V. Deliganis et al., Biochem. Pharmacol. 41, 1739 (1991). (MerckIndex)
1992: In der Entheogen Review erscheinen viele Artikel ueber die Extraktion von DMT aus diversen Pflanzen oder Bereitungen von ayahuaska-Analoga mit DMT. (eigen)
1993: J. Ott publizierte "Pharmacotheon", eine ungemein perfekte und wissenschaftliche und umfassende Zusammenfassung ueber das Gebiet Halluzinogene. (eigen)
1995: J. Ott publizierte "Ayahuasca Analogues: Pangean Entheogens.", ein Buch ueber Ayahuasca-Analoga und DMT-haeltige Pflanzen. (eigen)
1995: A. und A. Shulgin publizieren "Tihkal", ihr Werk ueber Halluzinogene Tryptamine. DMT wird selbstverstaendlicherweise auch erwaehnt. (eigen)
Der Domainname www.erowid.org ist registriert worden. (Tryptamine Palace)
Goa Trance wird in Goa, Indien, gespielt und viel synthetisches LSD und extrahiertes DMT von austral. Acacias ist erhaeltlich. (Tryptamine Palace)
1996: Nicholas Sand ist einer von 7 Personen, arrestiert in Canada fuer das Betreiben eines der groessten LSD Labors in Nordamerika. 4kg DMT wurden auch gefunden. (Tryptamine Palace)
1997: "Tihkal" wird von A. und A. Shulgin publiziert. (eigen)
2001: Portugal erlaubt den Eigenkonsum aller Drogen. (Tryptamine Palace)
2009: "Tryptamine Palace" wird das erste Buch ueber 5-Methoxy-DMT. (Tryptamine Palace)
ca. 2010: Die Santo Daime-Kirche gewinnt in den Vereinigten Staaten ihre von der Verfassung garantierte Freiheit zurueck. Der oberste Gerichtshof entscheidet sich fuer die Religionsfreiheit. Eine der urspruenglichen Religionen der suedamerikanischen Ureinwohner erhaelt seine Rechte zurueck. (eigen)
2001: Dr. Rick Strassman, ein Professor an der Universitaet der "Mexico medical school", hat es geschafft den buerokratischen Dschungel von FDA, DEA und anderen Autoritaeten zu ueberleben. In 1991 leitete er das erste offizielle psychedelische Forschungsprogramm in den USA seit 1970. Im Jahr 2001 purblizierte Strassman seine Ergebnisse in 'DMT: The Spirit Molecule'. Er unternahm eine Reihe von klinischen Studien. (eigen)
Durch die Expansion von google und dem Internet verbreitet sich der Gebrauch von ayahuasca und DMT-haeltigen Pflanzen in jede Ecke der Welt. Pflanzenfirmen, die via Internet Ayahuasca-Analoga auf der Basis der natuerlichen Pflanzen versenden, schiessen wie Pilze aus dem Boden. Die Extraktionsverfahren werden vereinfacht und via Internet diskutiert. Synthesetexte von Analogs sind generell problemlos erhaeltlich. Jedem sein Tryptamin. (eigen)
2011: Amerika verbietet 5-Methoxy-DMT in Schedule I. (Tryptamine Palace)
2011: Australien verbietet jede DMT-beinhaltende Pflanze, egal wieviel DMT sie enthaelt. Damit verbietet Australien sogar seine eigene Wappenpflanze. Wiederum ein Stueck unglaublich-ignoranten Pflanzen-Genozids. Es werden uebrigens auch jeden Psilocin/Psilocybin-beinhaltende Pilzart verboten, jede Datura-Art, jede Brugmansia-Art, ...(eigen)
Abbildung 1: In: TRACHSEL Daniel, RICHARD Nicolas: "Psychedelische Chemie.", S. 353, Nachtschatten Verlag, Solothurn, 2000.