
(#3, #17, #62)
4-Hydroxy-DMT, (#23) 3- [2- (dimethylamino) ethyl]- 1H- indol -4- ol, 4-Hydroxy -N,N- dimethyltryptamin. (#62)
1H-Indol-4-ol, 3-[2-(dimethylamino)ethyl]-; Indol-4-ol, 3-[2-(dimethylamino)ethyl]-; CX 59; N,N-Dimethyl-4-Hydroxytryptamine; Psilocine; 4-Hydroxy-N,N-dimethyltryptamine; 3-(2-(Dimethylamino)ethyl)indol-4-ol; Psilotsin; 3-[2-(Dimethylamino)ethyl]-1H-indol-4-ol; Psilocin (Psilocyn or 4-Hydroxy-N,N-dimethyltryptamine). (NIST)
Der angegebene Dosisbereich schwankt von einer Startdosis von 5mg oral (#23) oder 6mg (#62) bis zur vollen Dosis von 10mg Psilocin. (#14)
A. Hofmann gibt die Dauer der halluzinogenen Wirkung mit 4-6h an.(#14)
Blaettchen aus MeOH, mp 173-176 Grad Celsius. (#62)
Freebase Psilocin:
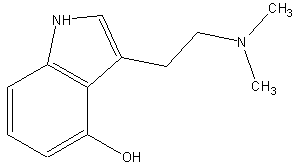
CAS Registry Number: 520-53-6
Summenformel: C12H16N2O (MERCK, DMT-Nexus, NIST, #62)
Molgewicht: 204.27 g/mol (MERCK, DMT-Nexus, #62)
Schmelzpunkt: 103-104 Grad Celsius (#101) , 173-176 Grad Celsius (Merck Index, #62)
XLogP3: 2.1 (PubChem)
Stabilitaet/Abbau: Unstabil in Loesung, speziell alkalische Loesungen (Merck Index).
Loeslichkeit:
Loeslich in 70% Ethanol. Schlecht loeslich in trockenem Ethanol, und schlecht loeslich in Ethanol mit weniger als 60%. Sehr leicht loeslich in Wasser (Quellen: Merck Index , scientific publications)(DMT-Nexus)
Leicht loesl. in H2O, loesl. in MeOH, EtOH, CHCl3. (#62)
Copelandia cyanescens;
Gymnopilus pupuratus;
Inocybe aeruginascens;
Panaeolus cyanescens, P. sphinctrinus, P. subbalteatus;
Pluteus salicinus;
Psilocybe baeocystis, P. caerulescens, P. cubensis, P. cyanescens, P. mexicana, P. pelliculosa, P. semilanceata, P. stuntzii;
Psilocin kommt in fast allen halluzinogenen Pilzen der Familien Psilocybe (Kahlkoepfe), Panaeolus (Duengerlinge) und Copelandia (Samthaeubchen) vor. Die Gesamtwirkung der halluzinogenen Pilze dieser Familien setzt sich aus den unterschiedlichen, in den Pilzen enthaltenen Mengen an Psilocin, Psilocybin und Baeocystin zusammen. Die Rauschdroge ist sehr nahe mit Psilocybin und DMT verwandt. Entfernt man die Hydroxygruppe von Psilocin erhaelt man DMT. Wird hingegen die Hydroxygruppe durch eine Phosphoryloxygruppe ersetzt erhaelt man das Halluzinogen Psilocybin, das ist der Phosphatester von Psilocin. Die Droge gehoert somit von der chemischen Struktur zu den Tryptaminen. (eigen) Die Verbindung ist unbestaendig, (#39, #40) da sie leicht oxydiert wird. (#47) Deswegen wurde auch das Halluzinogen Psilocybin von der Fa. Sandoz angeboten und nicht Psilocin, welches luftdicht und in braunen lichtgeschuetzten Flaschen aufbewahrt werden muesste. (eigen) Die vom Menschen aufgenommene Gesamtmenge wird uebrigens beinahe unveraendert im Harn ausgeschieden. (#62)
Es aehnelt LSD in der Wirkung (#39) und wirkt gleich wie Psilocybin. (#13, #62) Die Verbindung ist aber 1,4x so potent wie Psilocybin. (#62) Psilocin ist von der Wirkung ein typisches Halluzinogen, und es ist mit den gleichen Gefahren, wie beim Konsum von Psilocybin zu rechnen. (eigen)
Alexander Shulgin fuehrt in seinem Buch Tihkal folgene Synthese fuer die Substanz an:
Zu einer Loesung von 0,5g 4-Acetoxyindol in 4ml Et2O, die geruehrt wurde und mit einem aeusseren Eisbad gekuehlt wurde, wurde tropfenweise eine Loesung von 0,5ml Oxalylchlorid in 3ml wasserfreiem Et2O hinzugefuegt. Das Ruehren wurde fuer eine halbe Stunde fortgesetzt und das Zwischenprodukt Indolglyoxylchlorid trennt sich als eine gelber, kristalliner Feststoff ab, wurde aber nicht isoliert. Es wurde dann tropfenweise eine Loesung von 40% Dimethylamin in Et2O hinzugefuegt, bis der ph-Wert einen Wert von 8-9 erreicht hatte. Die Reaktion wurde dann abgebrochen durch die Zugabe von 100ml CHCl3 und die organische Phase wurde mit 30ml 5%-iger NaHSO4-Loesung gewaschen, dann mit 30ml gesaettigter NaHCO3-Loesung und schliesslich mit 30ml gesaettigtem Salzwasser. Nach dem Trocknem mit wasserfreiem MgSO4 wurde das Loesungmittel im Vakuum entfernt. Der Rest bildete Kristalle und nach Umkristallisieren aus THF wurden 0,61g (80%) 4-Acetoxyindol-3-yl-N,N-dimethylglyoxylamid mit einem mp von 204-205 Grad Celsius erhalten.
Eine Suspension von 0,38g LAH in 10ml wasserfreiem THF wurde kraeftig in einer Inertathmosphaere gehalten und geruehrt. Zu dieser Suspension wurde tropfenweise eine Loesung von 0,55g 4-Acetoxyindol-3-yl-N,N-dimethylglyoxylamid in 10ml wasserfreiem THF mit einer Rate, dass ein gemaechliches Kochen am Rueckfluss moeglich wurde. Nachdem die Addition fertig war, wurde weitere 15 Minuten am Rueckfluss gekocht, dann abgekuehlt auf 40 Grad Celsius und das ueberschuessige Hydrid durch die Zugabe von etwas Wasser in ein wenig THF zerstoert. Die Reaktionsmischung wurde von unloeslichen befreit unter einer N2-Athmosphaere und die resultierenden Festoffe wurden mit THF gewaschen. Die Filtrate und Waschungen wurden verweint und vom Loesungsmittel im Vakuum befreit. Der Rest wurde in einem KugelRohr-Apparat destilliert und das feste Destillat wurde aus EtOAc/Hexan umkristallisiert, um 3-[2-(dimethylamino)ethyl]-4-indolol (Psilocin) als weisses Oel, welches sich verfestigte zu ergeben. Umkristallisieren aus EtOAc/Hexan ergab weisse Kristalle mit einem mp von 103-104 Grad Celsius. Das endgueltige Gewicht betrug 0,23g (56% Ausbeute). (#101/468)
Metoltest; (#51/73)
Die Ausbildung einer koerperlichen Abhaengigkeit ist nicht bekannt. (eigen)
Psilocin ist chemisch und von der Wirkung sehr nahe mit Psilocybin verwandt und deshalb kann man annehmen, dass die gleichen Methoden bei Notfaellen angesagt sind:
Mittel der ersten Wahl bei einer problematischen Psilocinerfahrung ist die positive Veraenderung der Umgebung. Ruhe, frische Luft und beruhigende Worte, die Methodik des "talk-downs", helfen einem Grossteil der Konsumenten ueber ihre schlechte Phase hinweg. Meistens sind es Aengste und verdraengte Inhalte frueherer Zeiten, die den Konsumenten bedraengen. Er kann sich aber auch durch die Umgebung, durch die starke Steigerung der Emotionalitaet die eben dem Halluzinogenrausch anhaftet, bedroht fuehlen. Das Auftreten negativer Eigen- und Fremdstimmungen und die Einnahme von Halluzinogenen an ungeeigneten Orten ist die Hauptursache von Problemen. T. Learys Theorie vom set und setting hat sich bestaetigt. Nur die Einnahme bei guter Grundstimmung und in der passenden Umgebung fuehrt zu einem positiven Erlebnis durch die Einnahme. Sollten aufarbeitungsnotwendige Erlebensinhalte reproduziert werden, ist es der erfahrene Begleiter, der diese therapeutisch aufarbeiten muss. Die erstmalige Einnahme von Halluzinogenen setzt erfahrene Begleitung voraus, um Schaeden zu verhindern. Eine Einnahme alleine ist nur fuer erfahrene Konsumenten problemlos.
Sollten die Umstaende lebensbedrohlich fuer den User oder die Umgebung werden, ist erst der Einsatz von Medikamenten gerechtfertigt. Es werden Anxiolytika, (z. Bsp. Tranxilium, Valium®, Rohypnol®) aus der Gruppe der Benzodiazepine, oder in extremeren Faellen auch klassische Neuroleptika verwendet werden. Gegen die Verwendung von alten Neuroleptika sprechen die starken Nebenwirkungen und bleibende Schaeden. Neuroleptika sind erst angezeigt, wenn verlaengerte Rauschzustaende auftreten, und man annehmen muss, dass durch die Einnahme des Halluzinogens eine psychotische Reaktion ausgeloest wurde. Eine halluzinogene Erfahrung stellt keine Modellpsychose dar, diese Vereinfachung und Negativauslegung von reproduzierten, traumatischen Materials, ist inzwischen nicht mehr zeitgemaess. Sollte es doch einer wieder einmal zuwege bringen, sein gesamtes Neurotransmittersystem durch derart ueberhoehte Dosen, schlechte Voraussetzungen, Stressoren, womoeglich noch andere bioaktive Stoffe, komplett durcheinanderzubringen, so dass man am besten nur mehr abwarten kann, dass sich alles wieder beruhigt, ohne irgendetwas applizieren zu koennen, was aufgrund der komplexen Situation erst recht zu einem verlaengerten neuronalen Chaos fuehrt.Die Verwendung des neuen d2/5-HT2-Antagonisten Risperidon kann erwogen werden, doch diese Verbindung ist noch nicht genuegend von uns untersucht worden, doch inzwischen gibt es viel spezifischere Serotoninrezeptorenblocker, die sicherlich viel spezifischer die entsprechenden Neurotransmittersysteme, die mit den veraenderten Wahrnehmungszustaenden verbunden sind, blockieren koennen. Es sind einige Serotonin-rezeptor-untertypen an bestimmten Orten im Gehirn wesentlich in der Erzeugung von der visuellen Symptome verwickelt, und gezielte Serotonin-Rezeptor-Untertypen-Blockerexperimente waeren noetig, um deren praktische Einsetzbarkeit zu evaluieren. (eigen)
1959: Isolation aus Psilocybe mexicana und Strukturaufklaerung durch Hofmann A. et al. (#17, #62)
1959: Synthese von Psilocin durch Hofmann A. (#62)
1960: Blaschko, Levine und Bocks sowie Horita und Weber untersuchten die biochemischen Reaktionen von Psilocybin und Psilocin in vitro. Sie stellten fest, dass nur Psilocin fuer die typische blaugruene Faerbung verantwortlich ist. Die Phosphatgruppe, die an der 4. Position des Tryptamingeruestes bei Psilocybin verankert ist, verhindert die Oxydation zu den Chinonen, die vermutlich die typischen Farbstoffe bilden. (#51/73)
1962: Isolation aus Psilocybe baeocystis durch Leung J. (#62)
Abbildung 1: In: TRACHSEL Daniel, RICHARD Nicolas: "Psychedelische Chemie.", S. 358, Nachtschatten Verlag, Solothurn, 2000.