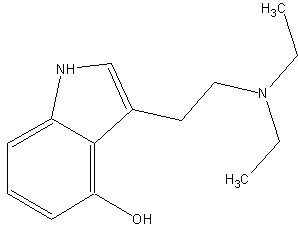

(#8, #45, #47)
4-Hydroxy-N,N-Diethyltryptamin, (#45, #47, #62) 3-[2-(diethylamino)ethyl]-1H-indol-4-ol, 4-Hydroxy-DET, Diethyl-4-Hydroxytryptamin. (#62) Ethocin; (Wikipedia)
TRYPTAMINE, N,N-DIETHYL-4-HYDROXY; 4-INDOLOL, 3-[2-(DIETHYLAMINO)ETHYL]; N,N-DIETHYL-4-HYDROXYTRYPTAMINE; 3-[2-(DIETHYLAMINO)ETHYL]-4-INDOLOL; CZ-74. (#101)
C14H20N2O, Mol. Gew. 232,45; Kristalle aus Aceton, mp 104-106 Grad Celsius. (#62)
Dieses Tryptamin ist ein synthetisches Halluzinogen, (#36, #45) dass nach der Entdeckung von Psilocybin und Psilocin, den hauptsaechlichen Wirkstoffen der halluzinogenen Pilze der Psilocybe-Familie und anderer halluzinogener Pilzfamilien durch den LSD-Entdecker A. Hofmann, bei der Firma Sandoz entwickelt wurde. Es ist strukturell nahe verwandt mit diesen Pilzwirkstoffen und gehoert zu den halluzinogenen Tryptaminen. Es ist ein Abkoemmling des DET, einem ebenfalls halluzinogenen Tryptamin. Der einzige Unterschied in der chemischen Struktur zwischen beiden Halluzinogenen ist, dass CZ-74 eine Hydroxygruppe an der Position 4 hat. Es ist damit chemisch sehr nahe mit diesem verwandt. CZ-74 ist eben 4-Hydroxy-DET. Wenn man nun diese 4-HO-Gruppe mit einer Phophophorylgruppe ersetzt erhaelt man den Phosphatester von 4-Hydroxy-DET, der unter dem Namen CEY-19 bekannt ist. Auch Psilocybin ist ein Phosphatester. Diese Verbindungen sind damit sehr aehnlich in der chemischen Struktur. Beide, CEY-19 und Psilocybin, koennen diese Phosphat-gruppe verlieren, vermutet man und wirken als 4-Hydroxy-DET im Koerper. Doch dies sind Spekulationen. Hineinschauen koennen wir nicht, wie der amerikanische Biochemiker A. Shulgin treffend in seinem Buch Tihkal anmerkte. Tatsache ist, dass alle vom 4-Hydroxy-DET abgeleiteten Ester (Phosphat, Acetat, Sulfat) wirksam sind, ebenso natuerlich das Esterfreie Hydroxyd, eben das 4-Hydroxy-DET, das ein Phenol ist. Der Acetatester wurde von A. Shulgin ebenfalls erstellt und getestet und erwies sich als wirksam. Der Sulfatester wurde uebrigens, scheint es, noch nicht am Menschen getestet worden zu sein. Da waere noch was zu tun...(eigen)
Die Wirkungen sind gleich wie bei Psilocybin, (#47) und es aehnelt damit auch LSD und Meskalin. (#36) Man muss annehmen, dass die Verbindungen zueinander eine Kreuztoleranz besitzen. Ob es, wie manche andere Tryptamine, eine Steigerung des Blutdruckes bewirkt, ist nicht bekannt. (eigen)
Die Dosis soll 10mg betragen. (#62)
10 - 25 mg, oral (als the Indolol, Acetat oder Phosphat). (#101)
Die Wirkdauer ist mit 3,5h (#45) verhaeltnismaessig lang fuer ein halluzinogenes Tryptamin. (eigen)
A. Shulgin fuehrt in seinem Buch Tihkal die Wirkdauer mit 4 - 6 h an. (#101)
Die Ausbildung einer koerperlichen Abhaengigkeit ist nicht bekannt geworden. (eigen)
Zu einer Loesung von 5.0 g 4-Hydroxyindol in 20 mL Pyridin wurde 10 mL Essigsaeureanhydrid hinzugefuegt und die Reaktionsmischung wurde auf dem Dampfad 10 Min. lang erhitzt. Die Reaktion wurde abgebrochen in dem man sie ueber zerstossenes Eis goss zu dem ein Ueberschuss an NaHCO3 hinzugefuegt wurde. Nachdem eine halbe Stunde geruehrt wurde, wurde das Produkt extrahiert mit Ethylacetat und die Extrakte wurden mit Salzwasser gewaschen und das Loesungsmittel wurde unter Vakuum entfernt. Der Rest wog 6.3 g (95%) dass, nach Umkristallisieren aus Cyclohexan, einen Schmelzpunkt von 98-100 Grad Celsius hatte.
Zu einer Loesung von 0.50 g 4-Acetoxyindol in 4 mL Et2O, dass geruehrt und abgekuehlt wurde mit einem externen Eisbad, wurde tropfenweise eine Loesung von 0.5 mL Oxalylchlorid in 3 mL wasserfreiem Et2O hinzugefuegt. Das Ruehren wurde 0.5 h lang fortgesetzt und das Zwischenprodukt Indolglyoxylchlorid separierte als ein gelber und kristalliner Feststoff, aber es wurde nicht isoliert. Es wurde dann tropfenweise eine 40%-ige Loesung von Diethylamin in Et2O hinzugefuegt, bis der pH-Wert 8-9 betrug. Die Reaktion wurde dann abgebrochen durch die Addition von 100 mL CHCl3, und die organische Phase wurde mit 30 mL 5%-iger NaHSO4 Loesung, mit 30 mL gesaettigter NaHCO3 Loesung, und schliesslich mit 30 mL gesaettigter Salzloesung gewaschen. Nach dem Trocknen mit wasserfreiem MgSO4, wurde das Loesungsmittel unter Vakuum entfernt. Der Rest bildete Kristalle und, nach Umkristallisieren aus Et2O, ergab es 0.62 g (72%) 4-Acetoxyindol-3-yl-N,N-diethylglyoxylamid mit einem Schmelzpunkt von 150-151 Grad Celsius.
Eine Suspension von 0.5 g LAH in 10 mL wasserfreiem THF wurde in einer Inertatmosphaere gehalten und kraeftig geruehrt. Zu diesem wurde tropfenweise eine Loesung von0.6 g 4-Acetoxyindol-3-yl-N,N-diethylglyoxylamid in 10 mL wasserfreiem THF hinzugefuegt mit einer Rate, die das Kochen am Rueckfluss ermoeglichte. Nachdem die Addition abgeschlossen war, wurde das Kochen am Rueckfluss fuer zusaetzliche 15 Min. aufrechterhalten, abgekuehlt auf 40 Grad Celsius, und das ueberschuessige Hydrid zerstoert durch die Addition von 1.0 mL EtOAc, gefolgt von 2.3 mL H2O. Die Reaktionsmischung wurde frei von Feststoffen filtriert unter einer N2 Atmosphaere, und gewaschen mit THF, und die Filtrate und Waschingungen wurden vereint und befreit vom Loesungsmittel unter Vakuum. Der Rest wurde in einem Kugelrohrapparat destilliert und die festen Stoffe wurden aus EtOAc/Hexan umkristallisiert, um 0.24 g (52%) 3-[2-(diethylamino)ethyl]-4-indolol (4-HO-DET) als weisse Kristalle mit einem Schmelzpunkt von 103-104 Grad Celsius´zu ergeben. Das Produkt entfaerbte sich schnell in der Gegenwart von Luft, und wurde am besten unter einer Inertathmosphaere -30 Grad Celsius gelagert. Umwandlung zum Phosphatester wurde durch die Reaktion des Natriumsalzes von 3-[2-(diethylamino)ethyl]-4-indolol mit Dibenzylchlorophosphonat erreicht, gefolgt von dem reduzierenden Entfernen der Benzylgruppe durch katalytische Hydrierung, wie es fuer Psilocybin beschrieben worden ist. (#101)
1959: Troxler et al. stellten CZ-74 dar. (#45, #62)
1965: Leuner und Baer testeten CZ-74 am Menschen. (#45)